Die Akute Myeloische Leukämie (AML) ist eine bösartige Blutkrebsform, die aus unreifen Vorstufen roter Blutkörperchen, Blutplättchen und einem Teil der weißen Blutkörperchen entsteht. Im Erwachsenenalter ist es die häufigste akute Leukämie. Bei etwa einem Drittel aller Patienten ist eine Veränderung des Wachstumsrezeptors FLT3 die Ursache für die unkontrollierte Teilung der bösartigen Zellen. Die Krebsmedizin verfolgt daher unterschiedliche Strategien diesen veränderten Rezeptor therapeutisch anzugreifen, z.B. mit Hemmstoffen oder mit Antikörpern der Krebsimmuntherapie.Ein solcher Antikörper wurde kürzlich im Deutschen Konsortium für Translationale Krebsforschung (DKTK) entwickelt und befindet sich jetzt in der klinischen Prüfung am Tübinger Universitätsklinikum. Der FLT3-Antikörper markiert Leukämiezellen, die nach zunächst scheinbar erfolgreicher Chemotherapie im Körper verbleiben. Die markierten Blutkrebszellen werden dann von den körpereigenen Abwehrzellen erkannt und gezielt abgetötet.
„Die Immuntherapie mit dem FLT3-Antikörper allein ist jedoch nicht immer erfolgreich“, erklärt Philipp Greif, DKTK Nachwuchsgruppenleiter am Klinikum der Universität München (LMU). „In manchen Fällen ist der FLT3-Rezeptor so verändert, dass er größtenteils von der Oberfläche der Leukämiezellen verschwindet und dadurch für den Antikörper gar nicht fassbar ist.“
In einer gemeinsamen Studie untersuchten die Tübinger und Münchner Wissenschaftler die Möglichkeit, die Blutkrebsform AML durch die Kombination beider Wirkstoffe zu heilen.
Sie nutzen spezielle Hemmstoffe, sogenannte Kinase-Inhibitoren, um den mutierten FLT3-Rezeptor wieder an die Zelloberfläche zu bringen und für die Immuntherapie wieder angreifbar zu machen. Dadurch konnten deutlich mehr AML-Zellen eliminiert werden. „Die Kombination der beiden Behandlungen wirkte in unseren prä-klinischen Modellen deutlich besser, als nur ein Wirkstoff allein“, sagt Katrin Reiter, Erstautorin der Studie.
Sowohl FLT3-Inhibitoren als auch FLT3-Antikörper sind in der klinischen Erprobung bereits weit fortgeschritten. Vor kurzem wurde der FLT3-Inhibitor Midostaurin für die AML-Therapie in Kombination mit einer Standard-Chemotherapie zugelassen. Folgestudien sollen jetzt zeigen, welche der verfügbaren Inhibitoren für die Kombination mit der FLT3-gerichteten Immuntherapie am geeignetsten sind.
Originalpublikation:
Reiter et al., Tyrosine kinase inhibition increases the cell surface localization of FLT3-ITD and enhances FLT3-directed immunotherapy of acute myeloid leukemia, Leukemia advance online publication 12 September 2017; doi: 10.1038/leu.2017.257
http://www.nature.com/leu/journal/vaop/ncurrent/full/leu2017257a.html
Förderung:
Das Projekt wurde durch die DFG gefördert (SFB 1243 Cancer Evolution)
Ein Bild zur Pressemitteilung steht zur Verfügung unter:
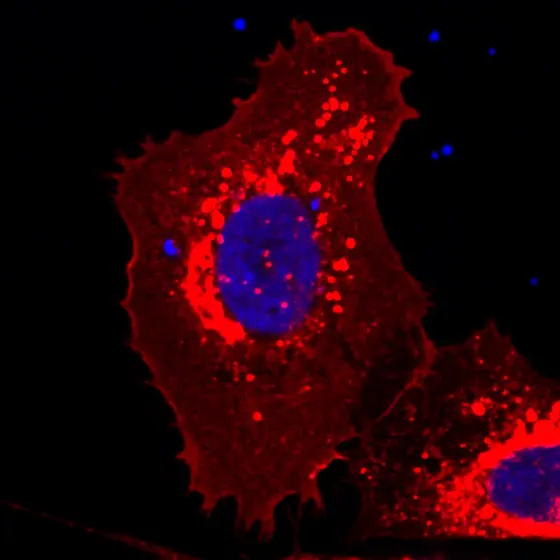
U2OS-ITD-EC28-TKI-blue-red.jpg
BU: Die Behandlung mit dem Inhibitor bringt den mutierten FLT3-Rezeptor (rot) wieder an die Zelloberfläche.
Nutzungshinweis für Bildmaterial zu Pressemitteilungen
Die Nutzung ist kostenlos. Das Deutsche Krebsforschungszentrum (DKFZ) gestattet die einmalige Verwendung in Zusammenhang mit der Berichterstattung über das Thema der Pressemitteilung bzw. über das DKFZ allgemein. Als Bildnachweis ist folgendes anzugeben: „Quelle: Reiter et al.; © 2017 Macmillan Publishers Limited, part of Springer Nature“
Eine Weitergabe des Bildmaterials an Dritte ist nur nach vorheriger Rücksprache mit der DKFZ-Pressestelle (Tel. 06221 42 2854, E-Mail: presse@dkfz.de) gestattet. Eine Nutzung zu kommerziellen Zwecken ist untersagt.
*Das Deutsche Konsortium für Translationale Krebsforschung (DKTK) ist eine gemeinsame, langfristige Initiative des Bundesministeriums für Bildung und Forschung (BMBF), der beteiligten Bundesländer und des Deutschen Krebsforschungszentrums (DKFZ) und wurde als eines der sechs Deutschen Zentren der Gesundheitsforschung (DZGs) gegründet. Im DKTK verbindet sich das Deutsche Krebsforschungszentrum (DKFZ) als Kernzentrum langfristig mit onkologisch besonders ausgewiesenen universitären Partnerstandorten und Kliniken in Deutschland. Mit dem DKFZ kooperieren Forschungseinrichtungen und Kliniken an Standorten Berlin, Dresden, Essen/Düsseldorf, Frankfurt/Mainz, Freiburg, Heidelberg, München und Tübingen, um optimale Bedingungen für die kliniknahe Krebsforschung zu schaffen. Das Konsortium fördert interdisziplinäre Forschungsthemen an der Schnittstelle zwischen Grundlagenforschung und Klinik, sowie klinische Studien zu innovativen Therapie- und Diagnoseverfahren. Ein weiterer Schwerpunkt ist der Aufbau von Forschungsplattformen, um den Einsatz personalisierter Krebstherapien zu beschleunigen und die Diagnose und Prävention von Krebserkrankungen zu verbessern.