Virus-assoziierte Karzinogenese
- Immunologie, Infektion und Krebs

Prof. Dr. Ralf Bartenschlager
Unsere Abteilung wurde im März 2014 gegründet, um die Mechanismen der Tumorbildung bei viralen Infektionen zu untersuchen. Dabei liegt der Schwerpunkt auf Leberkrebs, welcher weltweit eine der häufigsten Ursachen für krebsbedingte Todesfälle ist.

Unsere Abteilung
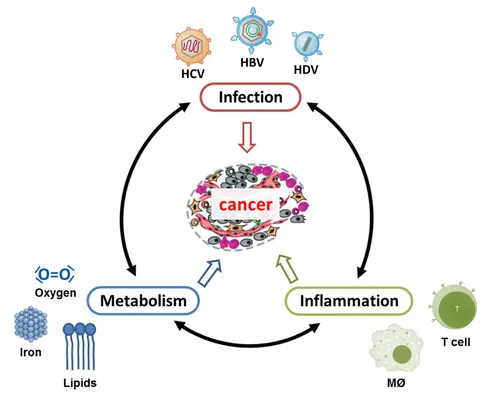
Etwa 75% aller an Leberkrebs erkrankten Patienten sind mit dem Hepatitis-C-Virus (HCV), dem Hepatitis-B-Virus (HBV) oder mit HBV und dem Hepatitis D Virus (HDV) infiziert. Dementsprechend ist der Leberkrebs ein Beispiel für eine Tumorart, die in hohem Maße mit Virusinfektionen assoziiert ist. Sie ist medizinisch sehr relevant, da weltweit ca. 60 Millionen Menschen mit HCV und ca. 250 Millionen mit HBV (darunter ca 5% zusätzlich mit HDV) infiziert sind. Die Wahrscheinlichkeit, dass sich bei diesen Personen ein Lebertumor entwickelt, wird durch vielfältige Faktoren begünstigt, wobei Stoffwechselstörungen, Alkoholmissbrauch oder chronische Entzündungen eine wesentliche Rolle spielen. Da die Behandlung von Lebertumoren derzeit nur begrenzt möglich ist, besteht ein dringender Bedarf an verbesserten Therapieansätzen sowie sensitiven diagnostischen Verfahren.
Gemeinsam mit unserer Schwester-Abteilung „Molekulare Virologie“ an der Universitätsklinik Heidelberg wurde bereits der Grundstein zur Erforschung von HBV, HDV, HCV und verschiedenen anderen RNA Viren gelegt und ein führendes Zentrum im Bereich der viralen Grundlagenforschung geschaffen. Angesichts der Ähnlichkeiten in wichtigen zellbiologischen Aspekten haben wir außerdem Studien zum Vermehrungszyklus des SARS-CoV-2 (Schweres Akutes Respiratorisches Syndrom Coronavirus-2) mit dem Ziel integriert, umfassend wirksame antivirale Medikamente zu entwickeln.
Aufbauend auf dieser Expertise forschen wir in der Abteilung "Virus-assoziierte Karzinogenese" am Deutschen Krebsforschungszentrum zu folgenden Schwerpunkten:
- Die Mechanismen, wie persistente Hepatitis-Virusinfektionen entstehen, wie eine chronische Infektion zur Entwicklung von Leberkrebs beiträgt und wie neuartige Konzepte zur Unterbrechung der viralen Persistenz entwickelt werden können, um das Krebsrisiko zu verringern
- Die grundlegenden Prinzipien, wie Virusinfektionen vom Körper erkannt und bekämpft werden, wie Viren diese antiviralen Abwehrmechanismen überwinden und welche Rolle die zelleigene antivirale Signalübertragung bei der Tumorentwicklung und -therapie spielt
- Die Etablierung eines Portfolios onkolytischer Parvoviren und die Analyse der Wechselwirkungen zwischen Virus und Wirtszelle im Zusammenhang mit virusinduzierten Zellstörungen
- Die Suche nach neuen, mit Tumoren beim Menschen assoziierten Viren mithilfe neuer bioinformatischer Methoden
- Die virologischen und immunologischen Determinanten der COVID-19-Pathogenese und die Nutzung der gewonnenen Erkenntnisse für eine verbesserte Vorbereitung auf zukünftige Pandemien. Diese Arbeiten wurden im Zuge der COVID-19-Pandemie aufgenommen und sie erfolgen im Rahmen des von der Helmholtz-Gesellschaft geförderten Forschungsnetzwerks „CoViPa“.
Ausführliche Informationen über die in den einzelnen Forschungsgruppen unserer Abteilung durchgeführten Forschungsarbeiten finden Sie auf deren Websites:
Arbeitsgruppe Ralf Bartenschlager
Arbeitsgruppe Marco Binder
Arbeitsgruppe Jürg Nüesch
Arbeitsgruppe Stefan Seitz
CoViPa Forschungsnetzwerk
Außerdem gehören folgende eigenständige Einheiten zu unserer Abteilung:
Arbeitsgruppe Stella Autenrieth
Arbeitsgruppe Timo Bund
Arbeitsgruppe Barbara Leuchs
Team
- Profil anzeigen

Prof. Dr. Ralf Bartenschlager
-
Sophie Bender
- Profil anzeigen

Dr. Marco Binder
-
Dr. Sandra Bühler
- Profil anzeigen

Liubov Chuprikova
- Profil anzeigen

Aditi Dhawan
- Profil anzeigen

Marius Flörchinger
-

Veronika Frehtman
- Profil anzeigen

Anne-Charlotte Gerstenberg
-
Leon Hennecke
-
Dr. Lisa Häfele
-
Doroteja Ilic
-
Lena Koch
-

Barbara Leuchs
-
Prof. Dr. Martin Löchelt
-
Anthi Maslarinou
-
Maria del Pilar Milla Picon
-
Dr. Giulia Mizzon
- Profil anzeigen

Kerstin Mohr
-
Paula Mostert
-

Marcus Müller
-
Dr. Firat Nebioglu
- Profil anzeigen

Dr. Jürg Nüesch
- Profil anzeigen

Gael Palais
-
Claudia Plotzky
-
Ilka Rebhan
- Profil anzeigen

Aleksandr Refeld
- Profil anzeigen

Theresa Schindler
Administration
- Profil anzeigen

Willram Scholz
-
Dr. Moritz Schüßler
-
Dr. Stefan Seitz
- Profil anzeigen

Sebastian Stegmaier
-
Alicia Weeber
-
Katrin Woll
- Profil anzeigen

Sandra Wüst
Scientific Project Management
- Profil anzeigen

Shangqing Yang
Ausgewählte Publikationen
Bonadonna M. et al.
Cortese M. et al.
Gillich N. et al.
Zander D. Y. et al.
Kontaktieren Sie uns



