Informationstechnologie
Dr. Claudia Galuschka


Im DKFZ ist die Informationstechnologie (IT) eine Grundvoraussetzung für die Arbeit der Mitarbeiterinnen und Mitarbeiter. Dies ist insbesondere auf moderne Labortechniken im Bereich der Genomanalyse wie auch durch die radiologische Bildverarbeitung mit ihren großen Datenmengen jeweils im Petabyte-Bereich zurückzuführen. Um aus Forschungsdaten relevante Informationen und Erkenntnisse zu gewinnen sind elaborierte Technologien notwendig. Aber auch die Durchdringung des normalen Arbeitsalltags mit Kommunikationstechnik und Büroanwendungen ist nach wie vor steigend, und Gebäudeüberwachung und Verwaltungsanwendungen werden zunehmend digitalisiert. Der Aspekt der IT Sicherheit spielt durch die Verarbeitung von personenbezogenen Daten in vielen Bereichen des Hauses eine bedeutende Rolle und wird in vielen nationalen und internationalen wissenschaftlichen Projekten und Kooperationen eingefordert. Aber nicht nur Vertraulichkeit und Integrität der Daten und Anwendungen sind wichtig, auch die Verfügbarkeit der IT ist für den Betrieb essentiell. Die IT hat damit eine tragende Rolle als „enabling technology“ für die Lebenswissenschaften und insbesondere für die Krebsforschung.
Die zentrale Einheit für Informationstechnologie (ITCF) hat als Aufgabe, IT im DKFZ optimal einzusetzen, die Mitarbeiter aus allen Bereichen des Hauses bei der Auswahl der IT-Tools für ihre jeweiligen Problemstellungen im Gesamtzusammenhang zu beraten, zentrale IT-Services zu implementieren und zu betreiben, sowie Lösungen für Fachabteilungen bei Projektierung und Betrieb zu unterstützen. Dies geschieht auf einer service-orientierten Basis. Es werden alle wesentlichen strategischen und operativen Funktionen und Aufgaben im DKFZ durch die ITCF maßgeblich unterstützt.
Arbeitsgruppen

Die AG Anwendungsentwicklung programmiert Applikationen für alle Bereiche des DKFZ. Primär sind das Webapplikationen in Verbindung mit Datenbanken, die auf den zentralen Servern der IT Core Facility gehostet werden. Wir erstellen auch die passenden APIs (Programmierschnittstellen), um den Datenaustausch von Drittprogrammen auf Quelltext-Ebene zu ermöglichen.

Die AG Desktop Services betreibt die Service-Zentren für Benutzeranfragen, bearbeitet Themen aus dem Desktop-Umfeld wie auch mobile Endgeräte und betreibt das Hochqualitätsdruck-Zentrum.

Die AG IT-Sicherheit ist für die operative Überwachung der IT-Sicherheit am DKFZ sowie für die Einführung, Weiterentwicklung und den Betrieb von Diensten und Prozessen zur Prävention von IT-Sicherheitsvorfällen und der Reaktion hierauf zuständig (Computer Emergency Response Team -CERT).

Die AG Netz ist für die gesamte Datennetzinfrastruktur des DKFZ und seiner Standorte zuständig. Dies umfasst neben der klassischen LAN-Anbindung eines Arbeitsplatzes auch die Ausleuchtung und Bereitstellung einer flächendeckenden Wireless LAN-Umgebung.
Hinzu kommen die Planung und der Betrieb der Netzinfrastrukturen in den verschiedenen Rechenzentren sowie deren Vernetzung und Übergängen. Aber auch Security Services und Zonenübergänge im Firewall-Segment fallen in diesen Verantwortungsbereich, ebenso wie die Anbindung an das Internet und die Integration von Partnerstandorten.
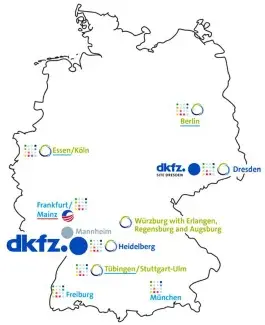
Die AG Partnerstandorte unterstützt die translationalen Standorte und Netzwerke des DKFZ (DKFZ-Dresden, DKTK, HECTOR, HI-TRON, NCT-Erweiterung) bei IT-relevanten Fragestellungen sowie bei der Planung, dem Aufbau und Betrieb der IT-Anbindung an das Kernzentrum in Heidelberg. Darüber hinaus ist die Arbeitsgruppe Ansprechpartner für die Koordinatoren an den Standorten und zentralen Koordinierungsstellen der Partnerstandorte am DKFZ.

Die AG Server und Compute betreibt zentrale Plattformen und Infrastrukturen des wissenschaftlichen Rechnens (SCI). Dazu gehört derzeit der Betrieb der DKFZ Cloud, basierend auf Openstack, der Cloud Umgebung für das deutsche Netzwerk Bioinformatik Infrastruktur de.NBI und in enger Kollaboration mit der ODCF ein Cluster zum wissenschaftlichen Rechnen auf Grafikkarten (GPGPU). Zentrale Server, Mail- und Fileservice, Druckdienste, Datensicherung, wie auch das wissenschaftliche Rechnen sind Themengebiete.

In der AG Softwaresysteme werden zentrale IT-Softwaresysteme und Dienste zur Verfügung gestellt. Dazu gehören Benutzerverwaltung, Softwareverteilung und Lizenzüberwachung, Berechtigungs- und Ressourcen-Management im Fileservice, Datenbankservice, Dokumentenmanagement und das elektronische Laborbuch.
Leitungsteam
-
Dr. Claudia Galuschka
Leiterin der Abteilung
-
Jürgen Trauth
AG Anwendungsentwicklung
-
Michael Cop
AG Desktop Services
-
Jan Tölken
AG IT-Sicherheit
-
Nils Kückenhoff
AG Netz
-
Heidrun Binder
AG Partnerstandorte
-
Markus Hohenhaus
AG Server und Compute
-
Heiko Rosenfelder
AG Softwaresysteme
TÜV IT-Zertifizierung
Für das DKFZ ist die Sicherheit der IT und der Daten von höchster Priorität. Deshalb wurde eine Zertifizierung des Haupt-Data Center durch die TÜV Informationstechnik GmbH durchgeführt. Diese umfaßt die baulichen Gegebenheiten, Brandmelde- und Löschtechnik, Sicherheits- und Zutrittssysteme, Energieversorgung, Klimatisierung und Organisation.
Das Data Center wurde nach Trusted Site Infrastructure TSI 3.2 Level 1 (erweitert) zertifiziert. Für die Elemente, die Sicherheit und Organisation anbelangen, wurden alle Kriterien des Katalogs erfüllt, die auch einem höheren Level genügen.
Auch für alle weiteren Data Center, die in Betrieb genommen werden, wird eine entsprechende Zertifizierung verlangt.
Weitere Informationen zu diesem Thema:
Internet-Zugang mit „eduroam“
Eduroam ist ein weltweiter Verbund von Universitäts- und Forschungsnetzen. Er ermöglicht es seinen Angehörigen an vielen Stellen der Welt, vor allem in Europa, mit ihrer persönlichen Benutzerkennung unkompliziert über WLAN Zugang zum Internet zu bekommen. Die WLAN-Kennung (SSID) lautet einheitlich „eduroam“.
Eduroam ist allein in etwa 200 Einrichtungen in Deutschland verfügbar, die Tendenz ist steigend.
Jeder DKFZ Mitarbeiter mit einer gültigen Benutzerkennung ist berechtigt eduroam zu nutzen. Um sich mit der ssid „eduroam" zu verbinden ist es zwingend notwendig das Profil zu installieren.
Windows, Android, iOS: https://www.geteduroam.app/ macOS: https://cat.eduroam.org/
Wird das Profil installiert muss sichergestellt sein, dass alle alten eduroam-Konfigurationen zuvor gelöscht wurden. Unter dem Reiter „Installationsanleitungen" finden Sie zu jedem Betriebssystem eine genaue Anleitung.
Der Dienst „eduroam“ gewährt Ihnen nur Zugriff auf das Internet. Zugriff auf das Intranet des DKFZ ist nur möglich, wenn Sie eine VPN-Verbindung aufbauen. Die Konfiguration des VPN-Zugangs auf Ihrem Rechner finden Sie im Intranet im Wiki der ITCF.
Eine Übersicht, sowie Listen der angeschlossenen Standorte, sind unter dem folgenden Link für Deutschland, Europa, Kanada und die USA abrufbar. In diese Listen sind jedoch nicht alle Standorte eingetragen, an denen eduroam verfügbar ist:
Für Nutzer von iPhone, iPad und Android-Geräte gibt es zudem die App „eduroam Companion“, zum Auffinden von eduroam-Standorten. Diese App ist in den jeweiligen App-Stores zu finden. Das DKFZ gibt jedoch keine Unterstützung für „eduroam Companion“ sowie für Android-Geräte im Allgemeinen.
Kontaktieren Sie uns

ITService
Core Facility ITPostanschrift: