Hirngenom-Mosaizismus und Tumorgenese
- Funktionelle und Strukturelle Genomforschung
- Nachwuchsgruppe

Dr. Pei-Chi Wei
Principal Investigator
Nicht alle Gehirnzellen haben die gleiche DNA. Einige dieser Veränderungen entstehen früh im Leben und könnten eine Rolle bei der Entstehung von Krankheiten wie Krebs spielen. Unser Labor untersucht, wie diese DNA-Veränderungen entstehen, wie sie an andere Zellen weitergegeben werden und wie sie sich im Gehirn ausbreiten.

Unsere Mission: Die Rolle der DNA-Vielfalt für die Gesundheit des Gehirns entschlüsseln
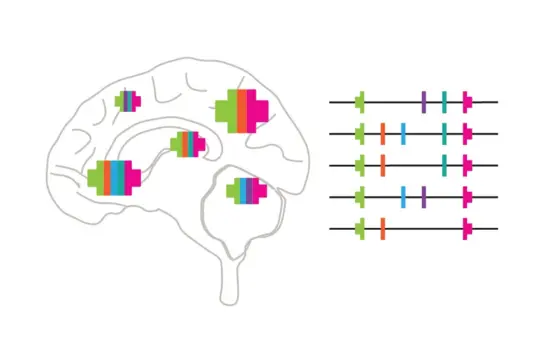
Die Entwicklung des Gehirns ist ein dynamischer Prozess
Das menschliche Gehirn besteht aus Milliarden von Neuronen und Astrozyten, die durch Hunderte von Teilungen neuraler Vorläuferzellen entstehen. Bemerkenswerterweise bilden sich die meisten dieser Zellen innerhalb von nur 24 Wochen während der fetalen Entwicklung. Dieser Prozess ist sowohl zeitlich als auch räumlich sorgfältig koordiniert und formt das etwa 400 g schwere Gehirn des Neugeborenen.
Mein Labor untersucht grundlegende Fragen: Woher wissen neurale Vorläuferzellen, wann sie aufhören müssen, sich zu teilen? Warum und wie verlängern sie ihre Zellzyklen? Führt die schnelle Zellteilung zu einer erhöhten DNA-Schädigung in diesen Zellen? Das Verständnis dieser Mechanismen ist entscheidend, um aufzudecken, wie Hirntumore entstehen, fortschreiten und sich entwickeln.
Methoden und Technologien
Wir haben experimentelle und analytische Werkzeuge entwickelt, um die Wechselwirkungen zwischen den zellulären Mechanismen aufzudecken, die für das Kopieren und Ablesen von DNA-Sequenzen verantwortlich sind. Mithilfe von Hochdurchsatz-Sequenzierungstechnologien messen wir den Zeitpunkt und die Geschwindigkeit der DNA-Replikation und untersuchen den transkriptionellen „Verkehr“, der durch die Mechanismen zur Entschlüsselung der DNA entsteht.
Darüber hinaus erstellen wir Mausmodelle, um zu untersuchen, wie neuronale Stammzellen während der frühen Gehirnentwicklung um Raum und Ressourcen konkurrieren. Zu unserer Arbeit gehört auch die Entwicklung experimenteller Systeme, die es uns ermöglichen, „in der Zeit zurückzureisen“ und das Verhalten neuronaler Stammzellen in frühen Entwicklungsstadien in späteren Lebensphasen nachzuverfolgen.
Ziele und gesellschaftliche Relevanz
Die Prävention von Hirntumoren steht vor erheblichen Herausforderungen, da unser Verständnis darüber, wie frühe zelluläre Prozesse dazu beitragen, begrenzt ist.
Forschungsprojekte

Der Aufbau eines Gehirns erfordert unzählige Zellteilungszyklen, und bei jeder Teilung müssen drei Milliarden Buchstaben unseres genetischen Codes originalgetreu kopiert werden. Manchmal gerät der Kopiermechanismus ins Stocken, und die lange DNA-Kette reißt. Wenn die Zelle die gebrochenen Enden falsch wieder zusammenfügt, gehen ganze Teile der genetischen Anweisungen verloren oder werden versehentlich dupliziert – ungeplante Verluste und Gewinne, die die Zelle nie vorgesehen hatte. Diese Veränderungen gehören zu den stärksten bekannten Risikofaktoren für Autismus und Hirntumore. Doch warum sie immer wieder an denselben Stellen auftreten, blieb bislang ein Rätsel.
In einer neuen Studie, die in Nature Communications veröffentlicht wurde, haben wir eine grundlegende Ursache identifiziert. Anhand der Stammzellen, aus denen das Gehirn entsteht, haben wir uns auf eine Handvoll „Schwachstellen“ im genetischen Code konzentriert. Diese befinden sich in den längsten Genen, die von Gehirnzellen genutzt werden – genau jenen Genen, die den Neuronen helfen, sich zu verbinden und miteinander zu kommunizieren – und sie reißen besonders leicht, wenn die DNA-Kopie ins Stocken gerät.
Wir haben gezeigt, dass diese Schwachstellen der Ausgangspunkt für die ungeplanten Verluste sind. Das Brechen selbst ist vorhersehbar – es geschieht jedes Mal an denselben Stellen, wenn die DNA-Kopie unter Stress steht –, die Reparatur jedoch nicht: Manche Zellen heilen sauber, manche verlieren immer wieder denselben Abschnitt und bilden so die bei Krankheiten beobachteten wiederkehrenden Veränderungen, und andere flicken den Schaden zu großen, einzigartigen Neuanordnungen zusammen, wodurch jedes Neuron einen leicht unterschiedlichen Satz genetischer Bausteine erhält. Dasselbe vorhersehbare Ereignis ist „Pech“ für Zellen, deren Reparatur
Übersetzt mit DeepL.com (kostenlose Version)
Unsere Forschung befasst sich damit, wie sich die Größe von neuronalen Stammzellklonen auf die Struktur und Funktion des Gehirns auswirkt. Neuronale Stammzellklone sind Gruppen von Neuronen, die denselben genetischen Bauplan teilen, und ihre Größe beeinflusst direkt die räumliche Organisation und die funktionelle Vielfalt der Neuronen im Gehirn. Interessanterweise zeigen Studien, dass die Größe neuronaler Klone je nach Hirnregion variiert, was darauf hindeutet, dass die Klongröße eine Schlüsselrolle dabei spielt, die Architektur des Gehirns an seine spezifischen Bedürfnisse anzupassen.
Mein Labor entwickelt präklinische Werkzeuge und Modelle, um die klonale Expansion, Selektion und Evolution im sich entwickelnden Gehirn zu untersuchen. Wir konzentrieren uns darauf, die Auslöser der klonalen Konkurrenz zu identifizieren – ein Prozess, der zu unkontrollierter, übermäßiger Zellproliferation führen kann, auch bekannt als präkanzeröse Hyperproliferation.
Unser Ziel ist es, festzustellen, ob eine solche unkontrollierte Proliferation in normalem Gewebe das Risiko einer Krebsentstehung erhöht. Letztendlich könnte diese Forschung neue Risikofaktoren aufdecken und Strategien zur Prävention von Hirntumoren liefern.
Team
Kurzer Beschreibungstext zur Vorstellung der Teammitglieder.
-

Dr. Pei-Chi Wei
Principal Investigator
-

Lorenzo Corazzi
Ph.D. student
-

Giulia Di Muzio
Ph.D. student
-

Boyu Ding
Ph.D. student
-

Mila Duerink
Masters student (Home Uni: Leiden, Leiden, NL)
-

Marco Giaisi
Lab Manager
-

Dr. Alex Ing
Senior Scientist
-

Hsin-Jui Lu
Ph.D. student
-
Maya Thomas
Masters student (Home uni: Sorbonne, Paris, FR)
Assoziierte Mitglieder
Michael Allers
M.D. student with Prof. Dr. Dr. Peter Huber (E055)
E-mail: m.allers(at)dkfz-heidelberg.de
Phone: +49 6221 42 3249
Ausgewählte Publikationen
Lorenzo Corazzi, Alex Ing, Eva Benito, Marco Raffaele Cosenza, Patrick Hasenfeld, Thomas Weber, Anna J. M. Marx, Vivien S. Ionasz, Nathan Trausch, Sarah Benedetto, Giulia Di Muzio, Boyu Ding, Jana Berlanda, Marco Giaisi, Nina Claudino, Thomas Höfer, Jan O. Korbel & Pei-Chi Wei
Giulia Di Muzio, Sarah Benedetto, Li-Chin Wang, Lea Weber, Franciscus van der Hoeven, Brittney Armstrong, Hsin-Jui Lu, Jana Berlanda, Verena Körber, Nina Claudino, Michelle Krogemann, Thomas Höfer, Pei-Chi Wei
Corazzi L., Ionasz V.S., Andrejev S., Wang L.-C., Vouzas A., Giaisi M., Muzio D.M., Ding B., Marx A.J.M., Henkenjohann J., Allers M.M., Gilbert D.M. & Wei P.-C.
Craig J Anderson, Lana Talmane, Juliet Luft, John Connelly, Michael D Nicholson, Jan C Verburg, Oriol Pich, Susan Campbell, Marco Giaisi, Pei-Chi Wei, Vasavi Sundaram, Frances Connor, Paul A Ginno, Takayo Sasaki, David M Gilbert, Núria López-Bigas, Colin A Semple, Duncan T Odom, Sarah J Aitken, Martin S Taylor
Aseda Tena, Yuxiang Zhang, Nia Kyritsis, Anne Devorak, Jeffrey Zurita, Pei-Chi Wei (co-correspondence) Frederick W. Alt
Pei-Chi Wei, Amelia N Chang, Jennifer Kao, Zhou Du, Robin M Meyers, Frederick W Alt, Bjoern Schwer
Offene Stellen
Replikationsstress ist ein Kennzeichen von Krebs. Die Überexpression von Onkogenen, der Verlust von Tumorsuppressoren und andere, noch unbekannte Faktoren begünstigen naturgemäß die Entstehung von DNA-Brüchen durch Replikationsstress. Es wird vermutet, dass dieser endogene Replikationsstress nicht nur das Fortschreiten von Krebs vorantreibt, sondern auch dessen Evolution begünstigt. Paradoxerweise hat sich jedoch die Erhöhung des Replikationsstresses – durch gezielte Beeinflussung des DNA-Replikationsapparats – auch als wirksame Strategie zur selektiven Abtötung von Krebszellen herausgestellt.
Unser Labor sucht derzeit einen Doktoranden, der die Mechanismen untersucht, die diesem Achillesferse des Krebses zugrunde liegen: dem Replikationsstress. Wir haben sowohl computergestützte als auch experimentelle Werkzeuge entwickelt, um die molekularen Prozesse, die zu DNA-Brüchen im Genom von Krebszellen führen, mit einer Auflösung auf Einzelnukleotid-Ebene zu analysieren.
Für weitere Informationen wenden Sie sich bitte an den PI.
Wir suchen im Rahmen der DKFZ Marie Skłodowska-Curie MasterClasses einen Postdoktoranden/in. Bitte bewerben Sie sich bis zum 18. Mai 2026.
Kontaktieren Sie uns