CHS Nachwuchsgruppe Neuronale Signalwege und Morphogenese
Dr. Annarita Patrizi
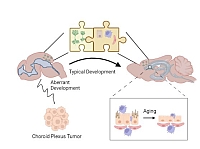
Die Entwicklung des menschlichen Gehirns ist ein langwieriger Prozess, der sich über das gesamte Leben erstreckt. Daher ist es wichtig zu verstehen, wie externe Umwelteinflüsse die Gehirnentwicklung und -reifung beeinflussen können. Jede umweltbedingte Störung dieser Prozesse kann eine Entwicklungsstörung des Nervensystems oder die Entstehung von Gehirntumoren auslösen. Unser Labor untersucht, wie intrinsische und extrinsische Faktoren die Entwicklung und Optimierung von Schaltkreisen im Gehirn beeinflussen. Eine wichtige Quelle von extrinsischen Signalen ist dabei der Plexus choroideus, eine einzigartige Schnittstelle zwischen dem Blut und der Zerebrospinalflüssigkeit. Wir wenden dabei biochemische, genetische, molekulare und anatomische Methoden sowie Verhaltensstudien an, um die instruktiven Signale in der Zerebrospinalflüssigkeit zu studieren und ihren Einfluss auf die Entwicklung der Gehirnschaltkreise und Plastizität zu ermitteln. Außerdem verwendet unsere Gruppe Tiermodelle, die Entwicklungsstörungen des Nervensystems und Gehirntumoren abbilden, um den möglichen Einfluss der Signale auf die Pathogenese der jeweiligen Krankheiten zu verstehen.
Unsere aktuelle und zukünftige Forschung befasst sich mit der Untersuchung der Mechanismen, die die Produktion und die Abgabe von spezifischen instruktiven Faktoren aus dem Plexus choroideus regulieren. Wir erforschen, wie diese Faktoren im Gehirn transportiert werden und wie diese Signale die normale und krankhafte Gehirnentwicklung und Plastizität beeinflussen. Eine Identifikation dieser Signalwege könnte wesentlich zum Erschließen der Plastizität des Gehirns und zur Prävention der Tumorentstehung beitragen.