Molekulare Hämatologie/Onkologie
- NCT
- Zell- und Tumorbiologie
- Klinische Kooperationseinheit

Prof. Dr. Alwin Krämer
90% der Krebstodesfälle in Deutschland werden durch Metastasen verursacht, sie stellen eine der größten Herausforderungen der Krebsforschung dar. Um Behandlungsergebnisse zu verbessern sind ein adäquates Verständnis der hochkomplexen Metastasierungsprozesse, sowie die Translation von Forschungsergebnissen in wirksame Behandlungsansätze erforderlich.
Bild: © dkfz.de, Bianca Kraft,
Bild: © dkfz.de, Bianca Kraft,
Unsere Forschung
Unsere translationale und klinische Forschung konzentriert sich auf Krebserkrankungen mit unbekanntem Primärtumor (Cancer of Unknown Primary, CUP). Das CUP-Syndrom ist eine hoch aggressive, primär metastatische Tumorerkrankung, bei der nur Metastasen, aber kein Primärtumor identifiziert werden kann. In Abwesenheit eines identifizierbaren Primärtumors sind die Behandlungsoptionen begrenzt. Patienten mit CUP-Syndrom haben eine dementsprechend ungünstige Prognose.
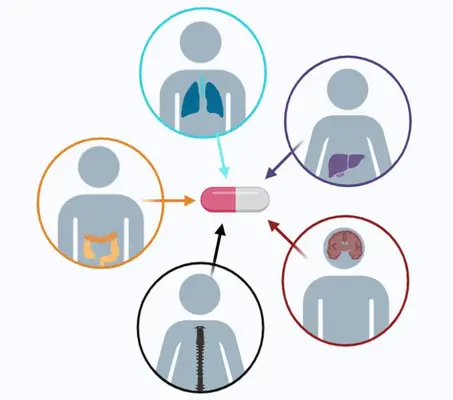
Aufgrund seines primär metastasierenden Verlaufes stellt das CUP-Syndrom eine für das Studium der Metastasierung paradigmatische Erkrankung dar und ermöglicht dadurch allgemeingültige Einblicke in die Mechanismen der Tumorprogression und Metastasierung, die weit über das CUP-Syndrom hinausgehen und auf andere Malignomentitäten übertragen werden können. Da das Organ der Tumorentstehung beim CUP-Syndrom unbekannt ist, dient die Tumorart zudem als eine Modellerkrankung für den Einsatz Primärtumor-agnostischer Therapien.
Auf dieser Basis zielt unsere Arbeit darauf ab, die Mechanismen der Metastasierung zu entschlüsseln, ausgehend von in vitro-Modellen und aufbauend auf Untersuchungen an primären Patientenproben (Tumorgewebe, Blut, Tumoroide), wobei die Ergebnisse stets mit klinischen Parametern verknüpft werden. Grundlagenwissenschaftlich befassen wir uns hauptsächlich mit Chromosomaler Instabilität (CIN) als einem der zentralen Mechanismen der Tumormetastasierung. Durch genomweite DNA-Sequenzierung, Transkriptom- und Methylomanalysen gewinnen wir wertvolle Erkenntnisse über molekulare Eigenschaften der Erkrankung und können maßgeblich zu biologischem Verständnis, Klassifikation und zielgerichteter Therapie des CUP-Syndroms beigetragen. Basierend auf diesen Daten und mit dem Ziel, die Behandlungsmöglichkeiten zu verbessern und innovative Strategien zur Überwindung von Therapieresistenz zu entwickeln, führen wir groß angelegte, multizentrische und internationale präzisionsonkologische Studien, sowohl für das neu diagnostizierte als auch für das rezidivierte oder therapierefraktäre CUP-Syndrom, durch.
Unsere Arbeit hat zur bislang weltweit größten randomisierten Phase-II-Studie bei Patienten mit CUP-Syndrom geführt, die kürzlich erstmals die Wirksamkeit Primärtumor-agnostischer, molekular zielgerichteter Therapien bewiesen hat. Dies stellt einen bedeutenden Meilenstein in der Behandlung des CUP-Syndroms und einen entscheidenden Schritt für die Integration der Präzisionsonkologie in die klinische Praxis dar.
Unsere Projekte im Detail
Die weiterführenden Seiten sind derzeit nur auf Englisch verfügbar:
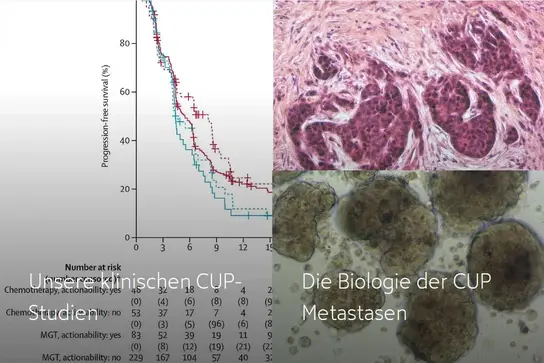
Unsere klinischen CUP Studien →
Die Biologie der CUP Metastasen →
Zukunftsperspektiven
Unsere zukünftigen klinischen Studien konzentrieren sich auf den Einsatz von Antikörper-Wirkstoff-Konjugaten, einem vielversprechenden Ansatz, der die Behandlung mehrerer Krebserkrankungen revolutioniert hat, beim rezidivierten oder therapierefraktären CUP-Syndrom.
Unter Verwendung von im Rahmen klinischer Studien gewonnenem primärem Patientenmaterial sowie davon etablierten Tumoroiden versuchen wir mittels Multi-Omics Ansätzen CUP-Tumore molekular zu profilieren und zu klassifizieren, die CUP-Biologie und Tumor-Wirt-Interaktionen zu verstehen sowie basierend auf Tumoroid-Modellen und High-Throughput Substanzscreens neue Substanzen zur Behandlung des CUP-Syndroms zu identifizieren und das Therapieansprechen vorherzusagen. Innerhalb eines integrierten Ansatzes, bei dem Forschung und klinische Praxis eng verknüpft werden, zielen wir darüber hinaus darauf ab, das Ursprungsgewebe von CUP-Syndromen zu bestimmen und dessen Einfluss auf die Therapieergebnisse zu untersuchen, um molekular fundierte Therapien zu ermöglichen.
Aufgrund der Primärtumor-agnostichen Natur des CUP-Syndroms werden wir die gewonnenen Daten letztlich dazu nutzen, die Nomenklatur von Tumorerkrankungen von einer rein klinisch-pathologischen Einteilung hin zu einer echten molekularen Klassifikation weiter zu entwickeln. So tragen wir zu innovativen Diagnose- und Behandlungsstrategien sowie zu besseren Behandlungsergebnissen für unsere Patienten bei.
Unser Team
Als Klinische Kooperationseinheit (KKE) sind wir eine gemeinsame Abteilung des Deutschen Krebsforschungszentrums (DKFZ) und der Abteilung Innere Medizin V des Universitätsklinikums Heidelberg, die sich sowohl mit der Erforschung als auch mit der Behandlung des CUP-Syndroms befasst.
Unser Team umfasst Wissenschaftler aus den Bereichen Humanmedizin, Data Science, Zell- und Molekularbiologie sowie Ärzte aus dem Universitätsklinikum und dem Nationalen Centrum für Tumorerkrankungen (NCT); unterstützt werden diese von hochmotivierten Studenten (PhD, MD Studenten) sowie biologisch- und medizinisch-technischen Assistenten.

Ausgewählte Publikationen
Pouyiourou M, Bochtler T, Pauli C, Moch H, Brobeil A, Pantel K, Stenzinger A, Krämer A
Krämer A, Bochtler T, Pauli C, Shiu KK, Cook N, Janoski de Menezes J, Pazo-Cid RA, Losa F, Robbrecht DGJ, Tomášek J, Arslan C, Özgüroğlu M, Stahl M, Bigot F, Kim SY, Naito Y, Italiano A, Chalabi N, Durán-Pacheco G, Michaud C, Scarato J, Thomas M, Ross JS, Moch H, Mileshkin L
Budczies J, Kazdal D, Menzel M, Beck S, Kluck K, Altbürger C, Schwab C, Allgäuer M, Ahadova A, Kloor M, Schirmacher P, Peters S, Krämer A, Christopoulos P, Stenzinger A
Pouyiourou M*, Kraft BN*, Wohlfromm T, Stahl M, Kubuschok B, Löffler H, Hacker UT, Hübner G, Weiss L, Bitzer M, Ernst T, Schütt P, Hielscher T, Delorme S, Kirchner M, Kazdal D, Ball M, Kluck K, Stenzinger A, Bochtler T, Krämer A
Krämer A, Bochtler T, Pauli C, Baciarello G, Delorme S, Hemminki K, Mileshkin L, Moch H, Oien K, Olivier T, Patrikidou A, Wasan H, Zarkavelis G, Pentheroudakis G, Fizazi K, on behalf of the ESMO Guidelines Committee
Kontaktieren Sie uns