Translationale funktionelle Krebsgenomik
- Funktionelle und Strukturelle Genomforschung
- NCT

Prof. Dr. Hanno Glimm
Tiefgreifende patientenspezifische Unterschiede in Bezug auf krebsverursachende Veränderungen sowie funktionelle Heterogenität innerhalb einzelner Tumore stellen die Entwicklung mechanismusbasierter Strategien in der klinischen Krebsbehandlung vor große Herausforderungen.

Unsere Forschung
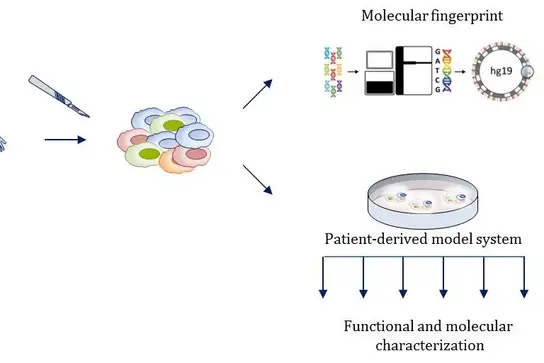
Die Forschung der Abteilung für Translationale funktionelle Krebsgenomik widmet sich der Entschlüsselung der komplexen Heterogenität von Tumoren. Durch umfassende genomische und funktionelle Analysen untersuchen Wissenschaftler und Ärzte der Abteilung patientenspezifische Unterschiede und die Diversität innerhalb von Tumorzell-Subpopulationen. Ziel ist es, das Verständnis für diese Variabilität zu vertiefen und daraus innovative, maßgeschneiderte Therapien zu entwickeln.
Um die Auswirkungen inter- und intratumoraler Heterogenität auf personalisierte Behandlungsansätze zu verstehen und anzuwenden, nutzen Wissenschaftler und Ärzte der Gruppe Translationale funktionelle Krebsgenomik ihre Erkenntnisse aus der mehrdimensionalen Analyse einzelner Tumorproben und Funktionstests von Patienten-abgeleiteten Tumormodellen, um neuartige Behandlungsstrategien zu identifizieren und zu validieren.
Aus Tumorproben von Patienten, welche im Rahmen des MASTER-Programms (Moleculary Aided Stratification for Tumor Eradication Research) ein umfassendes molekulares Profiling erhalten, werden individuelle Kulturen erzeugt, um funktionelle Eigenschaften zu untersuchen und Behandlungsstrategien zu testen. Mit unserem tiefgreifenden Fachwissen auf dem Gebiet der Stammzell- und molekularen Krebsbiologie untersuchen wir die Klonalität, Heterogenität sowie funktionellen Merkmale patientenspezifischer Primärtumore und der jeweiligen Modellsysteme. Dabei befassen wir uns besonders mit der klonalen Dynamik von einzelnen Subpopulationen in benignen und malignen Stammzellfraktionen. Tumorinitiierende Zellen benutzen sehr oft molekulare Mechanismen, die gutartige Stammzellsysteme regulieren, daher setzen wir gezielte Hochdurchsatz-Screening-Verfahren zusammen mit neuen Ansätzen aus der Einzelzellanalyse und Mausgenetik ein, um kritische und deregulierte Faktoren zu identifizieren, welche zu Tumorinitiierung, Metastasenbildung und Therapieresistenz führen. Verifizierte mechanistische Erkenntnisse werden wann immer möglich in klinische Behandlungsstrategien umgesetzt.
Die Gruppe Translationale funktionelle Krebsgenomik in Heidelberg arbeitet mit Wissenschaftlern der Abteilung Translationale Medizinische Onkologie in Dresden zusammen. So können beide NCT-Standorte ihre komplementären Stärken bei gemeinsamen translationalen Forschungsprogrammen erfolgreich einbringen.
Team
-

Maximilian Bullemer
-
Katharina Dreiling
-
Andreas Graur
-

Erik Kaiser
-
Haidar Kasem
-

Michael Wegert
-

Constantin Zehender
Ausgewählte Publikationen
Dieter, S. M.; Lovecchio, D.; Pataskar, A.; Zowada, M. K.; Körner, P.-R.; Khalizieva, A.; van Tellingen, O.; Jäger, D.; Glimm, H.; Agami, R.
Dieter, S. M.; Siegl, C.; Codó, P. L.; Huerta, M.; Ostermann-Parucha, A. L.; Schulz, E.; Zowada, M. K.; Martin, S.; Laaber, K.; Nowrouzi, A.; Blatter, M.; Kreth, S.; Westermann, F.; Benner, A.; Uhrig, U.; Putzker, K.; Lewis, J.; Haegebarth, A.; Mumberg, D.; Holton, S. J.; Weiske, J.; Toepper, L.-M.; Scheib, U.; Siemeister, G.; Ball, C. R.; Kuster, B.; Stoehr, G.; Hahne, H.; Johannes, S.; Lange, M.; Herbst, F.; Glimm, H.
Functional States in Tumor-Initiating Cell Differentiation in Human Colorectal Cancer
Zowada, M. K.; Tirier, S. M.; Dieter, S. M.; Krieger, T. G.; Oberlack, A.; Chua, R. L.; Huerta, M.; Ten, F. W.; Laaber, K.; Park, J.; Jechow, K.; Müller, T.; Kalxdorf, M.; Kriegsmann, M.; Kriegsmann, K.; Herbst, F.; Krijgsveld, J.; Schneider, M.; Eils, R.; Glimm, H.; Conrad, C.; Ball, C. R.
Perivascular Niche in the Bone Marrow Hosts Quiescent and Proliferating Tumorigenic Colorectal Cancer Cells.
Möhrmann, L.; Zowada, M. K.; Strakerjahn, H.; Siegl, C.; Kopp-Schneider, A.; Krunic, D.; Strunk, D.; Schneider, M.; Kriegsmann, M.; Kriegsmann, K.; Herbst, F.; Ball, C. R.; Glimm, H.; Dieter, S. M.
The Notch Target Gene HEYL Modulates Metastasis Forming Capacity of Colorectal Cancer Patient-Derived Spheroid Cells in Vivo
Weber, S.; Koschade, S. E.; Hoffmann, C. M.; Dubash, T. D.; Giessler, K. M.; Dieter, S. M.; Herbst, F.; Glimm, H.; Ball, C. R.
Systematic Generation of Patient-Derived Tumor Models in Pancreatic Cancer
Ehrenberg, K. R.; Gao, J.; Oppel, F.; Frank, S.; Kang, N.; Dieter, S. M.; Herbst, F.; Möhrmann, L.; Dubash, T. D.; Schulz, E. R.; Strakerjahn, H.; Giessler, K. M.; Weber, S.; Oberlack, A.; Rief, E.-M.; Strobel, O.; Bergmann, F.; Lasitschka, F.; Weitz, J.; Glimm, H.; Ball, C. R.
Mapping Active Gene-Regulatory Regions in Human Repopulating Long-Term HSCs
Wünsche P*, Eckert ESP*, Holland-Letz T, Paruzynski A, Hotz-Wagenblatt A, Fronza R, Rath T, Gil-Farina I, Schmidt M, von Kalle C, Klein C, Ball CR, Herbst F§, Glimm H§
NRG1 Fusions in KRAS Wild-Type Pancreatic Cancer
Heining C*, Horak P*, Uhrig S*, Codo PL, Klink B, Hutter B, Fröhlich M, Bonekamp D, Richter D, Steiger K, Penzel R, Endris V, Ehrenberg KR, Frank S, Kleinheinz K, Toprak UH, Schlesner M, Mandal R, Schulz L, Lambertz H, Fetscher S, Bitzer M, Malek NP, Horger M, Giese NA, Strobel O, Hackert T, Springfeld C, Feuerbach L, Bergmann F, Schröck E, von Kalle C, Weichert W, Scholl C, Ball CR, Stenzinger A, Brors B, Fröhling S§, Glimm H§
Genetic subclone architecture of tumor clone-initiating cells in colorectal cancer
Giessler KM*, Kleinheinz K*, Huebschmann D, Balasubramanian GP, Dubash TD, Dieter SM, Siegl C, Herbst F, Weber S, Hoffmann CM, Fronza R, Buchhalter I, Paramasivam N, Eils R, Schmidt M, von Kalle C, Schneider M, Ulrich A, Scholl C, Fröhling S, Weichert W, Brors B, Schlesner M, Ball CR, Glimm H
Pan-cancer analysis of somatic copy-number alterations implicates IRS4 and IGF2 in enhancer hijacking
Weischenfeldt J*, Dubash T*, Drainas AP*, Mardin BR, Chen Y, Stütz AM, Waszak SM, Bosco G, Halvorsen AR, Raeder B, Efthymiopoulos T, Erkek S, Siegl C, Brenner H, Brustugun OT, Dieter SM, Northcott PA, Petersen I, Pfister SM, Schneider M, Solberg SK, Thunissen E, Weichert W, Zichner T, Thomas R, Peifer M, Helland A, Ball CR, Jechlinger M, Sotillo R, Glimm H§, Korbel JO§
Kontaktieren Sie uns

