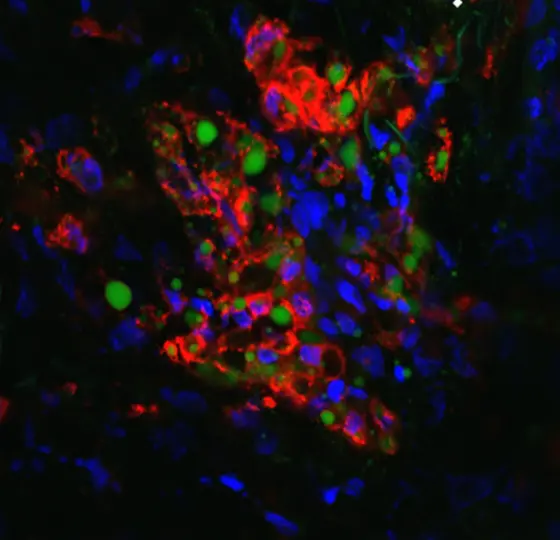
Eierstockkrebs und andere Tumorerkrankungen breiten sich häufig in das sogenannte Bauchnetz aus – eine fettreiche Gewebeschicht im Bauchraum, die die inneren Organe bedeckt und nicht immer einfach dem Begriff „Bauchfett“ entspricht. Das HI-TRON-Team um Niels Halama untersuchte, wie diese besondere Umgebung die Interaktion zwischen Tumorzellen und Immunzellen beeinflusst.
Dabei zeigte sich: In der Nähe von Tumorabsiedelungen (Metastasen) im Fettgewebe sammeln sich besonders viele Immunzellen, darunter T-Zellen und sogenannte tumorassoziierte Fresszellen (Makrophagen). Während die T-Zellen durch das Fettgewebe grundsätzlich funktionsfähig bleiben, geraten Makrophagen durch die Aufnahme großer Mengen an Fett unter oxidativen Stress. In diesem Zustand tragen sie zur Unterdrückung der Immunantwort bei und begünstigen so das Tumorwachstum.
Blockade bestimmter Signalwege reaktiviert die Immunabwehr
Die Forschenden konnten zeigen, dass sich dieser immununterdrückende Zustand der Makrophagen durch gezielte Eingriffe umkehren lässt.
In Experimenten mit Tumorgewebe von Patientinnen sowie in Mausmodellen führte die Hemmung des Signalwegs um den Rezeptor CCR5 – etwa mit dem Medikament Maraviroc – dazu, dass Makrophagen neu programmiert wurden. In der Folge konnten T-Zellen wieder stärker in den Tumor eindringen und Krebszellen wirksamer bekämpfen. Der bereits zugelassene Wirkstoff Maraviroc war ursprünglich für die Therapie von HIV-Infektionen entwickelt worden.
Einen ähnlichen Effekt beobachteten die Forschenden auch, wenn ein weiterer Entzündungs- und Fetttransport-Mechanismus über den Rezeptor CD36 blockiert wurde. Beide Ansätze reduzierten die Fettbelastung der Makrophagen und stärkten die entzündliche Immunantwort gegen den Tumor.
Welche Patientinnen profitieren besonders von der Immuntherapie?
Darüber hinaus liefert die Studie Hinweise darauf, welche Patientinnen besonders von Therapien mit Immun-Checkpoint-Inhibitoren profitieren könnten. In einer Analyse klinischer Daten zeigte sich, dass Fettgewebe eine doppelte Rolle spielt: Patientinnen mit Metastasen im fettreichen Bauchnetz sprachen häufiger auf Checkpoint-Inhibitoren an als Frauen, deren Tumor sich nicht in dieses Gewebe ausgebreitet hat.
Mit bildgebenden Verfahren und maschinellem Lernen konnten die Forschenden sogar ein Modell entwickeln, das anhand von CT-Aufnahmen das Vorliegen von Bauchnetz-Metastasen und damit die Wahrscheinlichkeit eines Therapieansprechens abschätzen kann.
„Die Ergebnisse machen deutlich, wie stark Stoffwechselprozesse im Tumorumfeld das Verhalten von Immunzellen beeinflussen. Dieser Einfluss bringt zugleich Vor- und Nachteile für die Patienten. Unsere Ergebnisse können dazu beitragen, dass wie diese Vorgänge in Zukunft bei Krebspatienten auch therapeutisch beeinflussen können“, sagt Studienleiter Niels Halama. Langfristig, so erwarten die Forscher, könnten Kombinationstherapien, die Immuncheckpoint-Inhibitoren mit Wirkstoffen gegen bestimmte Stoffwechsel- oder Entzündungssignale verbinden, die Behandlung von Eierstockkrebs und anderen Tumorerkrankungen verbessern. Auch Ernährung und Sport könnten sich günstig auswirken – Studienergebnisse dazu liegen allerdings noch nicht vor.
Publikation:
Meggy Suarez-Carmona et al.: Harnessing lipid-driven immunometabolic pathways in omental metastases to enhance immunotherapy in patients with ovarian cancer
Signal Transduction and Targeted Therapy 2026, https://rdcu.be/e6Ily
* HI-TRON Mainz wurde 2018 als Gemeinschaftsunternehmen des Deutschen Krebsforschungszentrums in Kooperation mit der TRON gGmbH, der Universitätsmedizin Mainz und der Johannes Gutenberg-Universität Mainz (JGU) gegründet. Das Institut verbindet die international herausragende Expertise dieser Partner auf dem Gebiet der personalisierten Immuntherapie in Mainz mit dem umfassenden Spektrum der Krebs-Spitzenforschung am DKFZ.