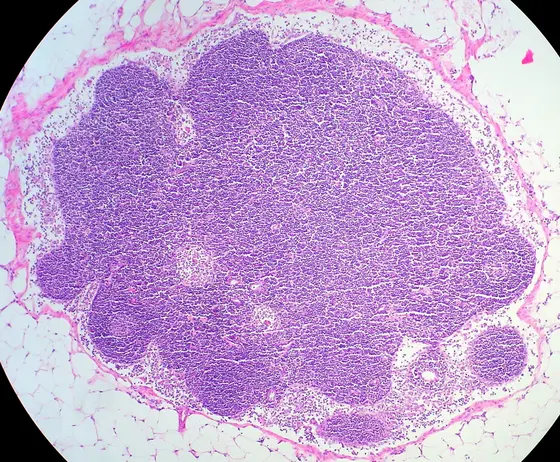
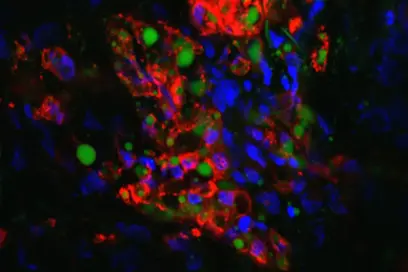
Lymphknoten sind zentrale Schaltstellen des Immunsystems und spielen eine wichtige Rolle in der Abwehr von Infektionen und Tumoren. Damit dies funktioniert, müssen Immunzellen (B-Zellen und T-Zellen) im Lymphknotengewebe räumlich exakt organisiert sein, etwa in sogenannte B-Zell-Follikel und T-Zell-Zonen. Gesteuert wird dies durch Stromazellen (nicht-blutbildende Stützzellen): Sie geben Botenstoffe ab und bilden damit Leitsignale, an denen sich Immunzellen orientieren, um ihre vorgesehenen Plätze im Lymphknoten zu finden.
Bei B-Zell-Lymphomen ist die innere Ordnung des Lymphknotengewebes je nach Erkrankung sehr unterschiedlich gestört: Während bei langsam wachsenden Lymphomen, z.B. dem follikulären Lymphom (FL), die grundlegende Gewebestruktur erhalten bleibt, bricht die räumliche Ordnung bei aggressiven Lymphomen, z.B. dem diffus-großzelligen B-Zell-Lymphom (DLBCL), vollständig zusammen. Warum diese typischen Wachstumsmuster entstehen, war bislang weitgehend unklar.
In der aktuellen Studie gelang es den Forschenden erstmals, diese Prozesse systematisch im menschlichen Lymphknoten darzustellen. Dabei konnten sie mithilfe von Einzelzell-Analysen und räumlicher Gewebekartierung nachzeichnen, welche Faktoren dazu führen, dass sich die Lymphknoten-Architektur bei Lymphomerkrankungen zunehmend auflöst.
Die Daten zeigen: Stromazellen sind die „Architekten“ des Lymphknotens. Die Forschenden konnten nachweisen, dass sich zentrale Leitsignale in spezialisierten Stromazellen bei von Lymphomerkrankungen grundlegend verändern und damit die räumliche Ordnung des Lymphknotens schrittweise zusammenbricht. Diese Veränderungen von Stromazellen spiegeln sich im Wachstumsmuster von Lymphomen wider: Während sich beim FL zwar die Größenverhältnisse von B-Zell-Follikeln und T-Zell-Zonen verschieben, die Bereiche aber überwiegend räumlich getrennt bleiben, gehen beim DLBCL wichtige Steuerungssignale und damit die Gewebestruktur weitgehend verloren.
Als treibenden Mechanismus identifiziert die Studie einen entzündlichen Teufelskreis: T-Zellen produzieren als Teil der Immunantwort im Tumorumfeld entzündungsfördernde Botenstoffe, sogenannte Interferone, die in Stromazellen zur Umstellung ihrer Botenstoff (Chemokin)-Produktion führen: Statt strukturgebender Signale dominieren entzündliche Chemokine, die wiederum weitere Entzündungszellen anziehen. Der Verlust der Lymphknoten-Organisation bei Lymphomen ist also kein passiver Effekt des Tumorwachstums, sondern wird aktiv durch Entzündungsprozesse in der Tumorumgebung vorangetrieben.
Bei Patientinnen und Patienten ist diese Umprogrammierung von Stromazellen mit schlechteren Überlebenschancen verbunden. Die Forschenden konnten in großen Patientengruppen zeigen, dass ein Verlust von strukturgebenden Chemokinen mit einer ungünstigen Prognose einhergeht.
Die Erkenntnisse ermöglichen auch neue potenzielle Therapieansätze. „Unsere Ergebnisse könnten für die Entwicklung neuer Therapien und für neue diagnostische Verfahren sehr wichtig sein“, so Daniel Hübschmann, DKFZ.
Quelle: Pressemitteilung des Universitätsklinikums Düsseldorf
Publikation:
Felix Czernilofsky et al.: Reprogramming of stroma-derived chemokine networks drives the loss of tissue organization in nodal B cell lymphoma
Nature Cancer 2026, DOI: 10.1038/s43018-026-01136-z