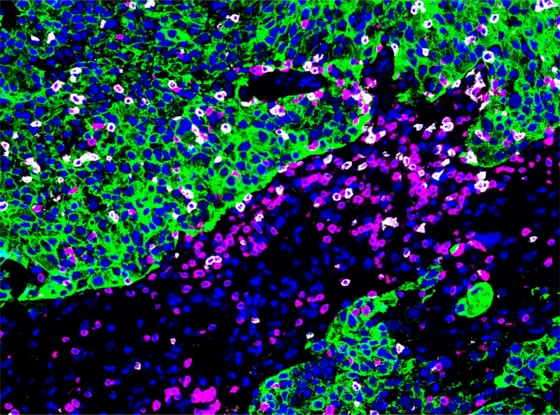
Wenn sich Krebszellen vom ursprünglichen Tumor in der Brust ablösen und im Gehirn Metastasen bilden, gibt es für die betroffenen Patientinnen bislang nur eingeschränkte Behandlungsmöglichkeiten. Hirnmetastasen gehen häufiger mit einer ungünstigeren Prognose einher als Metastasen in anderen Organen des Körpers. Es gibt daher großen Bedarf, die zellulären Wechselwirkungen in Hirnmetastasen besser zu verstehen und darauf aufbauend eine möglichst gezielte Therapie zu finden. In der nun veröffentlichten Studie untersuchte das Team von Heidelberger Forscherinnen und Forschern das zelluläre Umfeld von Hirnmetastasen bei insgesamt 156 Brustkrebspatientinnen, insbesondere die Abwehrzellen sowie weitere Zellen des Tumormikromilieus. Für eine möglichst detaillierte Analyse kombinierten sie mehrere Verfahren, um die Zellarten sowie deren Abwehrbereitschaft zu charakterisieren. Über eine räumliche Analyse konnte das Forschungsteam zudem nachvollziehen, wo im Gewebe viele abwehrbereite Immunzellen zu finden waren.
Zwei „Immunlandschaften“ gehen mit günstigerem Verlauf einher
Die Forschenden entdeckten bei der räumlichen Verteilung der Immunzellen Muster, die sie als „Immunlandschaften“ beschrieben. Befanden sich rund um die Metastase zum Beispiel nur wenige Immunzellen, die den Krebs bekämpften, war dieses Muster mit einer ungünstigen Prognose verbunden. Daneben identifizierte das Team zwei Immunlandschaften, bei denen sich ein günstigerer Verlauf für die Patientinnen zeigte. Das eine dieser beiden Muster wies eine hohe Zahl gewebeständiger Gedächtnis-T Zellen auf. Diese speziellen Abwehrzellen bleiben vermutlich im Gewebe, erkennen Tumorzellen offenbar wieder und können besonders rasch reagieren. Das zweite günstige Muster war durch organisierte Ansammlungen von Immunzellen im Tumorgewebe gekennzeichnet, die in ihrer Funktion kleinen Lymphknoten ähneln und eine Immunantwort gegen den Tumor unterstützen können.
Patientenzellen in der Kulturschale bestätigen die wichtige Rolle der T Zellen bei der Tumorkontrolle
„Das Besondere ist, dass wir nicht nur diese Muster, sondern auch ihre biologische Funktion beschreiben konnten“, so Lena Jassowicz, die Erstautorin der Studie. Um die Beobachtungen aus dem Metastasengewebe experimentell zu überprüfen, nutzte das Team patienteneigene Modelle. Dabei werden isolierte Tumor- und Immunzellen eines Menschen im Labor zusammengebracht, um ihre Wechselwirkung unmittelbar und ohne Störeinflüsse zu untersuchen. Es zeigte sich, dass die identifizierten gewebeständigen T Zellen die Tumorzellen der jeweiligen Patientin sehr effektiv angriffen und zerstörten. „Wir schließen aus diesen Ergebnissen, dass diese Zellen tatsächlich eine wichtige Rolle bei der Tumorkontrolle spielen“, sagt Fangyoumin Feng, DKFZ, ebenfalls Erstautorin.
Diese T Zellen könnten als Ansatzpunkt für eine gezielt wirkende Immuntherapie dienen. Immuntherapien verstärken die körpereigene Abwehrreaktion gegen Krebszellen. Allerdings profitieren nicht alle Patientinnen und Patienten gleichermaßen von einer solchen Behandlung. Deshalb werden Marker benötigt, anhand derer sich vorhersagen lässt, für wen eine solche Behandlung sinnvoll sein kann. Dazu liefert die Studie wichtige Hinweise: In ergänzenden Laborversuchen konnten die Forschenden außerdem zeigen, dass sich die Aktivität der T Zellen durch eine Immuncheckpoint-Blockade weiter steigern ließ.
Gensignaturen als Marker der Immunlandschaften
In einem weiteren Schritt leiteten die Forschenden aus ihren Ergebnissen charakteristische Muster aktiver Gene ab, die die zuvor identifizierten günstigen Immunlandschaften kennzeichnen. In Tests mit externen Datensätzen von Brustkrebspatientinnen zeigten diese Gensignaturen zuverlässig eine bessere Prognose an. Solche Signaturen könnten künftig genutzt werden, um Tumoren oder Metastasen molekular besser einzuordnen und die Therapieentscheidung zu unterstützen. So kann es auch hilfreich sein, immunologisch „kalte“ Metastasen zu identifizieren, die voraussichtlich kaum auf Immuntherapien ansprechen. Unnötige Belastungen durch eine wenig aussichtsreiche Behandlung könnten so vermieden werden. „Schon zu wissen, dass eine Patientin mit größerer Wahrscheinlichkeit eher von einer anderen Behandlung als der Immuntherapie profitieren wird, kann klinisch sehr wertvoll sein“, sagt Martina Seiffert, DKFZ.
„Die Arbeit liefert nicht nur neue Einblicke in die Biologie von Brustkrebs-Hirnmetastasen, sondern auch konkrete Anhaltspunkte für die Weiterentwicklung personalisierter Therapien“, sagt Sandro Krieg, Ärztlicher Direktor der Neurochirurgischen Universitätsklinik Heidelberg. Ein möglicher nächster Schritt wäre es, therapeutische Strategien in klinischen Studien zu erproben, um die vorhandenen Immunreaktionen gegen die Tumorzellen gezielt weiter zu verstärken. „Unsere Daten zeigen sehr klar, dass es sich lohnt, Hirnmetastasen als eigene biologische Einheit zu betrachten“, sagt Christel Herold-Mende, Universität Heidelberg und UKHD. „Nur wenn wir diese Besonderheiten verstehen, können wir Therapien präziser und damit hoffentlich wirksamer machen“, so Herold-Mende.
Quelle: Pressemitteilung des UKHD
Lena Jassowicz, Fangyoumin Feng, Rolf Warta, Fatima Heinicke, Amélie Wöllner, Hannah Briesch, Furkan Sor, Julia Soller, Catharina Lotsch, John K.L. Wong, Chang-Gyun Park, Nicolas Aubert, Maximilian Scheer, Zhaoqing Hu, Maximilian Knoll, Julian Schlegel, Lukas Frank, Philip Dao Trong, Gerhard Jungwirth, Amin I. Nohman, Kendra Maaß, Niels Grabe, Mandy Barthel, Simone Butz, Christina Lulay, Manuela Zucknick, Michele Bortolomeazzi, Pooja Sant, Verena Thewes, Laura Michel, Carlo Fremd, Andreas Schneeweiss, Chong Sun, Karsten Rippe, Amir Abdollahi, Andreas von Deimling, Andreas Unterberg, Sandro M. Krieg, Jan-Philipp Mallm, Peter Lichter, Marc Zapatka, Martina Seiffert, Christel Herold-Mende: Dissecting the cellular architecture of breast cancer brain metastases reveals prognostically distinct immune landscapes
Cancer Cell, 2026, DOI: 10.1016/j.ccell.2026.03.016
https://doi.org/10.1016/j.ccell.2026.03.016.