Wie alle Zellen in unserem Körper sind auch Krebszellen darauf angewiesen, ausreichend mit Nährstoffen und Sauerstoff versorgt zu werden. Beides erhalten sie über den Blutkreislauf. Da Krebszellen sich besonders schnell teilen, müssen in den Geschwüren auch schnell und teils unkontrolliert neue Blutgefäße wachsen. Könnte man diesen Prozess der Angiogenese hemmen, ließen sich das Tumorwachstum unterdrücken.
Wissenschaftler um Hellmut Augustin zeigen jetzt, dass der Rezeptor Tie1 dabei eine entscheidende Rolle spielt. Tie1 wird von Endothelzellen gebildet, also den Zellen, die das Innere unserer Blutgefäße auskleiden. Dieser Rezeptor arbeitet mit anderen Signalmolekülen zusammen und bewirkt, dass Blutgefäße kontrolliert wachsen. Augustin forscht am Deutschen Krebsforschungszentrum und am European Center for Angioscience, das an der Medizinischen Fakultät Mannheim der Universität Heidelberg angesiedelt ist.
In den Blutgefäßen innerhalb von Tumoren wird jedoch verstärkt Tie1 produziert. Das Wachstum der Blutgefäße und dadurch des gesamten Tumors beschleunigt sich. Dieser Effekt tritt zur Überraschung der Forscher allerdings erst in der späten Phase der Tumorentwicklung auf. Bei Mäusen ohne Tie1 wuchsen Tumoren zunächst in normaler Geschwindigkeit. Erst nach etwa zwei Wochen verlangsamte sich ihr Wachstum. Für die medizinische Anwendung könnte das vorteilhaft sein. „Wenn Tumoren diagnostiziert werden, ist ihre evolutionäre Entwicklung in den allermeisten Fällen bereits weit fortgeschritten“, erklärt Augustin. „Daher ist es wichtig, therapeutische Ziele zu identifizieren, die in dieser späten Phase der Tumorentwicklung wirkungsvoll angreifbar sind, wie wir es hier für Tie1 nachgewiesen haben.“
Tie1 hat noch einen weiteren Effekt: Es destabilisiert die Wände der Blutgefäße und fördert dadurch die Ausbildung von Metastasen. Metastasen sind verantwortlich für den Großteil der krebsbedingten Todesfälle. Solche Sekundärtumoren entstehen, wenn Krebszellen den Primärtumor verlassen, im Blutkreislauf mitschwimmen und sich dann an einem neuen Ort im Organismus niederlassen. Dort können sie wochen- oder sogar jahrelang in einer Art Ruhezustand verharren bevor sie erneut damit anfangen, sich unkontrolliert zu teilen. „Wir haben Tie1 in Endothelzellen genetisch ausgeschaltet und Tumorwachstum und Metastasierung unterdrückt“, erklärt Silvia La Porta, die Erstautorin der Studie. „Im nächsten Schritt werden wir untersuchen, ob wir durch medikamentöse Unterdrückung von Tie1 den gleichen Effekt erzielen können.“
Im Experiment an Mäusen zeigte sich, dass nach der Entfernung des Primärtumors 10 von 14 Kontrolltiere Metastasen aufwiesen. Bei genetisch veränderten Mäusen, deren Endothelzellen den Tie1 Rezeptor nicht bilden konnten, hatte jedoch nur 1 von 14 Tieren nachweisbare Metastasen.
Wie genau Tie1 wirkt, ist noch Gegenstand intensiver Forschung. Das Molekül ist ein sogenannter Orphan-Rezeptor, also ein Rezeptor, für den kein Bindungspartner bekannt ist. Zukünftige Studien sollen Licht ins Dunkel bringen.
Die Idee, das Wachstum von Blutgefäßen in Tumoren zu unterdrücken, ist nicht neu. 2005 kam der Wirkstoff Bevacizumab (Avastin) auf den Markt, der genau nach diesem Prinzip funktioniert: Er blockiert den Gefäßwachstumsfaktor VEGF und behindert damit die Angiogenese. Allerdings ist die Wirksamkeit von Bevacizumab begrenzt. Daher sind Wissenschaftler weltweit auf der Suche nach Molekülen, die gemeinsam mit Avastin angewandt werden können und als Kombinationstherapie eine verbesserte Wirksamkeit haben.
In den letzten Jahren haben Pharmafirmen vor allem das Molekül Angiopoietin2 genauer unter die Lupe genommen. Anders als Tie1 beeinflusst Angiopoietin2 jedoch vor allem die frühen Phasen der Tumorentwicklung. Aufgrund seines späteren Wirkungszeitraums könnte sich Tie1 als besserer Angriffspunkt erweisen.
Silvia La Porta, Lise Roth, Mahak Singhal, Carolin Mogler, Carleen Spegg, Benjamin Schieb, Xianghu Qu, Ralf H. Adams, H. Scott Baldwin, Soniya Savant, and Hellmut G. Augustin: Endothelial Tie1–mediated angiogenesis and vascular abnormalization promote tumor progression and metastasis.
Journal of Clinical Investigation 2018, DOI: 10.1172/JCI94674.
Ein Bild zur Pressmitteilung steht zum Download zur Verfügung:
PM-JCI-LaPorta-et-al.jpg
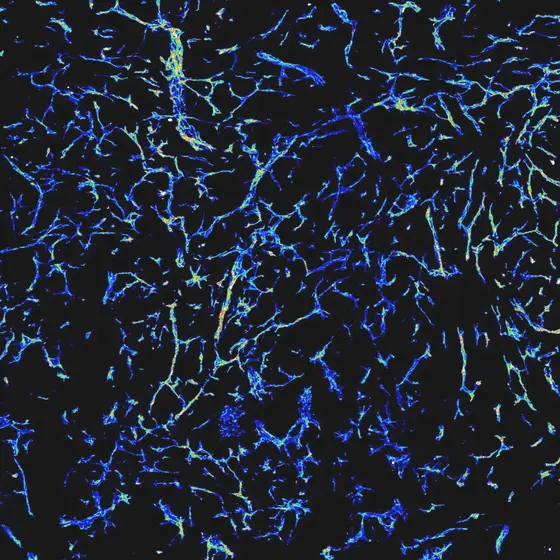
BU: Mikroskopische Darstellung des dichten Netzes von Blutgefäßen in einem wachsenden Tumor.
Nutzungshinweis für Bildmaterial zu Pressemitteilungen
Die Nutzung ist kostenlos. Das Deutsche Krebsforschungszentrum (DKFZ) gestattet die einmalige Verwendung in Zusammenhang mit der Berichterstattung über das Thema der Pressemitteilung bzw. über das DKFZ allgemein. Bitte geben Sie als Bildnachweis an: „Quelle: La Porta, DKFZ“.
Eine Weitergabe des Bildmaterials an Dritte ist nur nach vorheriger Rücksprache mit der DKFZ-Pressestelle (Tel. 06221 42 2854, E-Mail: presse@dkfz.de) gestattet. Eine Nutzung zu kommerziellen Zwecken ist untersagt.