„Zellen ein und desselben Tumors können genetisch sehr verschieden sein und dadurch auch unterschiedlich auf die Therapie reagieren“, erklärt Christine Sers von der Berliner Charité, Leiterin der im Wissenschaftsmagazin Nature Communications veröffentlichten Studie. Bislang war jedoch nicht bekannt, welchem räumlichen Muster diese genetischen Veränderungen genau folgen.
Um das herauszufinden, zerlegten die Wissenschaftler einen Darmtumor in 68 Proben aus unterschiedlichen Geweberegionen und analysierten die 100 am häufigsten veränderten Gene. Die räumliche Anordnung der genetischen Unterschiede rekonstruierten sie anschließend in einem dreidimensionalen Tumormodell. „Aufgrund der hohen Auflösung war es möglich, auch genetische Veränderungen zu erkennen, die nur in einem sehr geringen Prozentsatz der Tumorzellen vorliegen“, betont Soulafa Mamlouk, Erstautorin der Studie.
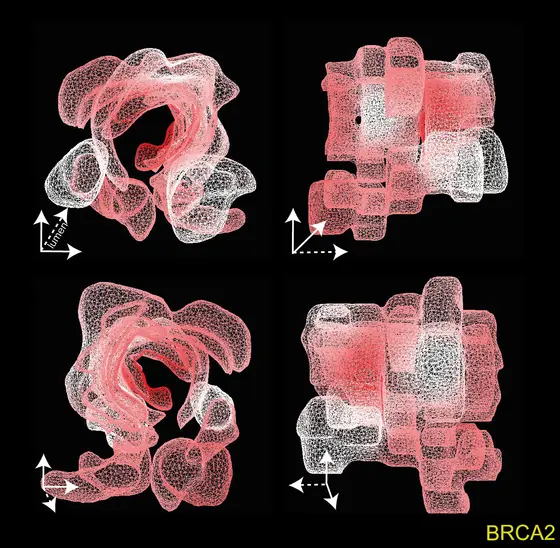
Interessanterweise unterschieden sich die einzelnen Tumorabschnitte kaum in der Art und Anzahl von Erbgut-Mutationen, sondern hauptsächlich in der Kopienzahl bestimmter Gene, die in den Zellen verringert oder vervielfacht wurden. Zahlreiche Genvervielfachungen fanden die Wissenschaftler beim Übergang vom äußeren zum inneren Tumorbereich, unter anderem für das Gen BRCA2, das bei Brustkrebs eine entscheidende Rolle spielt. Auch in der invasiven Tumorregion, jenem Areal, das in angrenzendes gesundes Gewebe hineinwächst, fanden die Wissenschaftler besonders viele Genvervielfältigungen, beispielsweise für das Gen HDAC2, das ein zentrales Enzym in der Genregulation kodiert.
Je nach Stadium unterschieden sich die Tumoren genetisch hauptsächlich durch die Anzahl bestimmter Genkopien. Das zeigte sich, als die Wissenschaftler jeweils den Primärtumor und verschiedene Metastasen von 27 Patienten verglichen. Gene wie CDX2 und WFDC2, welche die Metastasenbildung und das Tumorwachstum begünstigen, waren in den Metastasen vervielfacht, während das Tumorsupressorgen SMAD4 dort in besonders geringer Kopienzahl vorlag.
„Unsere Ergebnisse sind ein wichtiger Hinweis darauf, dass Tumorprogression und Therapieverhalten entscheidend durch Genvervielfältigung und Genverlust bestimmt werden“, sagt Christine Sers. „Tumorzellen, bei denen ganze Chromosomenabschnitte oder einzelne Gene vervielfacht wurden, sind genetisch besonders anpassungsfähig und werden möglicherweise auch schneller gegen Therapien resistent.“ Die Studie zeigt außerdem, dass gängige Biopsien nicht immer Aufschluss über alle Tumormerkmale geben. Die Ergebnisse der Wissenschaftler könnten dabei helfen, differenziertere Tumorprofile zu erstellen und die derzeitige Routinediagnostik zu verbessern.
Mamlouk, S. et. al.: DNA copy number changes define spatial patterns of heterogeneity in colorectal cancer. In: Nature Communications (25. Januar 2017) Doi:10.1038/ncomms14093
Bilder und ein Video zur Pressemitteilung stehen zum Download zur Verfügung unter:
BRCA2-rotation.jpg
Supplementary-movie.gif
BU Bild:
Das dreidimensionale Tumormodell zeigt, in welchen Arealen die Kopienzahl des Gens BRCA2 im Darmtumor verändert ist. Im inneren Tumorbereich fanden die Wissenschaftler besonders viele Kopien des Gens (dunkelrot), während in einigen äußeren Regionen die Kopienzahl kaum zunahm (hellrot) oder unverändert blieb (weiß).
BU Video:
Rotierender Darmtumor in 3D: Zwei unterschiedliche Gencluster (grün und violett) zeigen im Darmtumor räumlich getrennte Muster der Genvervielfältigung.
Nutzungshinweis für Bildmaterial zu Pressemitteilungen
Die Nutzung ist kostenlos. Das Deutsche Krebsforschungszentrum (DKFZ) gestattet die einmalige Verwendung in Zusammenhang mit der Berichterstattung über das Thema der Pressemitteilung bzw. über das DKFZ allgemein. Als Bildnachweis ist folgendes anzugeben: „Quelle: Christine Sers, Soulafa Mamlouk / Charité Berlin“
Eine Weitergabe des Bildmaterials an Dritte ist nur nach vorheriger Rücksprache mit der DKFZ-Pressestelle (Tel. 06221 42 2854, E-Mail: presse@dkfz.de) gestattet. Eine Nutzung zu kommerziellen Zwecken ist untersagt.