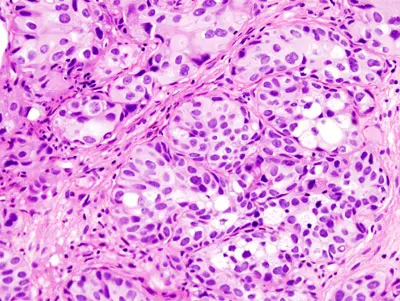
Im Deutschen Krebsforschungszentrum hatten Wissenschaftler um Dr. Rajiv Kumar kürzlich beim bösartigen schwarzen Hautkrebs eine weitverbreitete Erbgutveränderung entdeckt. Die Mutation betrifft die als „Unsterblichkeitsenzym“ bezeichnete Telomerase. Um die Bedeutung dieser Erbgut-Veränderung bei anderen Krebsarten aufzuklären, analysierten die Forscher nun gemeinsam mit Kollegen vom schwedischen Karolinska-Institut das Tumorerbgut von 327 Blasenkrebs-Patienten. Bei 65 Prozent der Tumoren entdeckten sie die identische Veränderung.
Bei der Zellteilung schützt die Telomerase die Enden der Chromosomen vor dem Abbau und damit die Zelle vor Alterung und Tod. Durch die Mutation entsteht in der Schalterregion (Promotor) des Telomerase-Gens eine Bindungsstelle für Proteinfaktoren, die das Gen übermäßig aktivieren. Als Folge bilden die mutierten Zellen vermehrt Telomerase und erlangen dadurch quasi Unsterblichkeit.
Patienten, deren Tumorerbgut die Mutation enthält, hatten einen ungünstigeren Krankheitsverlauf und der Krebs kehrte nach Behandlung häufiger zurück. Dies galt aber nicht generell, sondern nur, wenn zusätzlich an einer anderen Stelle des Telomerase-Genschalters eine bestimmte „Schreibweise“ vorlag. Solche alternativen Schreibweisen an einzelnen Erbgut-Positionen werden als Polymorphismen bezeichnet.
Nur Patienten, mit der häufigeren, „normalen“ Schreibweise waren vom ungünstigen Effekt der Telomerase-Mutation betroffen. Bei Trägern der selteneren, varianten Version machte sich der Effekt dagegen kaum bemerkbar. Die Forscher vermuten, dass die seltenere Schreibweise den aktivierenden Effekt auf die Telomerase wieder aufhebt.
Rajiv Kumar geht davon aus, dass während der Krebsentstehung Zellen mit der aktivierenden Mutation im Telomerase-Promoter begünstigt sind: „Weil sie sich so häufig teilen, sind Tumorzellen von der Telomerase abhängig, um ihr Erbgut intakt zu halten.“
Die Bedeutung der Telomerase für Krebszellen ist wiederum eine Chance, Blasenkrebs mit neuartigen Medikamenten zu behandeln. Wirkstoffe gegen die Telomerase sind bereits entwickelt, einige werden sogar schon in klinischen Studien der Phase III geprüft. Eine Blockade des Unsterblichkeitsenzyms kann möglicherweise auch das Wachstum von Blasenkrebs bremsen. Außerdem sehen Kumar und Kollegen in der Kombination aus Mutation und Genvariante einen vielversprechenden Biomarker, der den Verlauf der Erkrankung vorhersagt.
Die Mutation im Telomerase-Promotor wurde bei 65 Prozent aller Blasenkrebs-Fälle, bei 74 Prozent der Melanome sowie bei 83 Prozent aller Glioblastome entdeckt. „Die meisten Erbgut-Analysen konzentrieren sich bei der Suche nach krebsfördernden Mutationen auf die proteinkodierenden Bereiche des Genoms“, sagt Rajiv Kumar. „Das erklärt, warum diese extrem häufige Mutation erst so spät entdeckt wurde.“
P. Sivaramakrishna Rachakonda, Ismail Hosen, Petra J. de Verdier, Mahdi Fallah, Barbara Heidenreich, Charlotta Ryk, Peter Wiklund, Gunnar Steineck, Dirk Schadendorf, Kari Hemminki und Rajiv Kumar: TERT promoter mutations in bladder cancer affect patient survival and disease recurrence through modification by a common polymorphism. Proceedings of the National Academy of Sciences, USA, 2013, DOI: 10.1073/pnas.1310522110