Therapiemonitoring neuer Therapieprotokolle zur Patientenstratifizierung
- 1. Longitudinale PET-CT-Studien mit FDG bei Patienten mit metastasierten Melanomen unter Immuntherapie
- 2. Longitudinale PET-CT-Studien mit FDG bei Patienten mit nicht resektablen Lungentumoren unter Immuntherapie oder kombinierter Chemo-Immuntherapie sowie bei resektablen Lungentumoren im neoadjuvanten Setting
- 3. Randomisierte multizentrische Phase III Studie zur Bewertung einer Induktionstherapie mit Lenalidomid, Bortezomib und Dexamethason mit entweder intravenös oder subkutan verabreichtem Isatuximab(GMMG HD-8-Studie)
- 4. Longitudinale PET-CT-Studien mit FDG bei Patienten mit Lymphomen unter CART-Zelltherapie
1. Longitudinale PET-CT-Studien mit FDG bei Patienten mit metastasierten Melanomen unter Immuntherapie
Auf der Suche nach zuverlässigen Biomarkern zur Überwachung und Vorhersage des Ergebnisses einer Immuntherapie untersuchen wir prospektiv die potenzielle Rolle von 18F-FDG-PET/CT bei der Behandlung von Melanompatienten, die mit verschiedenen Immuncheckpoint-Inhibitoren (ICIs) wie CTLA-4-, PD1- und LAG-3-Inhibitoren oder deren Kombinationen behandelt werden. Um diese Probleme anzugehen, werden verschiedene Bewertungsmethoden und Erfassungsprotokolle von PET/CT verwendet und Längsschnittstudien zu verschiedenen standardisierten Zeitpunkten während der Behandlung durchgeführt. Ihre Validierung basiert auf klinischen Langzeit- und Überlebensdaten der Patienten.
Die grundlegenden Forschungsfragen, mit denen sich dieses Projekt beschäftigt, sind folgende:
- Bedeutung von 18F-FDG PET/CT im frühen Behandlungsverlauf zur Vorhersage des langfristigen Ansprechens auf eine Immuntherapie bei metastasiertem Melanom
- Neuartige Ansätze und spezielle immunbezogene Antwortkriterien zur zuverlässigen Interpretation der 18F-FDG PET/CT-Immuntherapieantwort
- Verwendung von 18F-FDG PET/CT als zuverlässiger Marker für das Absetzen einer Immuntherapie
- Visualisierung und Bedeutung immunbezogener Nebenwirkungen
- Prognostischer Wert der 18F-FDG-Aufnahme in lymphatischen Organen wie der Milz sowie deren Veränderungen während der Immuntherapie
Kooperation mit Prof. Dr. med. Jessica Hassel, Klinik für Dermatologie und Nationales Centrum für Tumorerkrankungen (NCT) und Universitätsklinikum Heidelberg
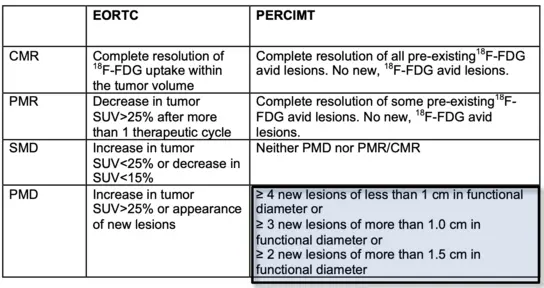
Abb. 1a. „Gemeinsame praktische Leitlinien von EANM/ANZNM/Verfahrensstandards von SNMMI für den empfohlenen Einsatz der [18F]FDG-PET/CT-Bildgebung während immunmodulatorischer Behandlungen bei Patienten mit soliden Tumoren“ Ver. 1.0 (Lopci E et al. Eur J Nucl Med Molecular Imaging 2022; 49:2323-2341)
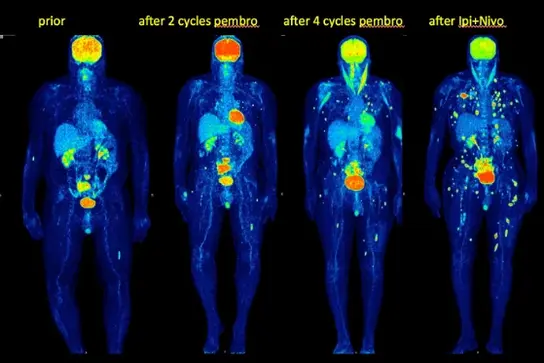
Abb. 1b. Definition neuer Kriterien für die Überwachung der Immuntherapie mit FDG-PET-CT-PET-Response-Evaluationskriterien für die Immuntherapie (PERCIMT) (Anwar H et al. Eur J Nucl Med Molecular Imaging 2018; 45:376-383)
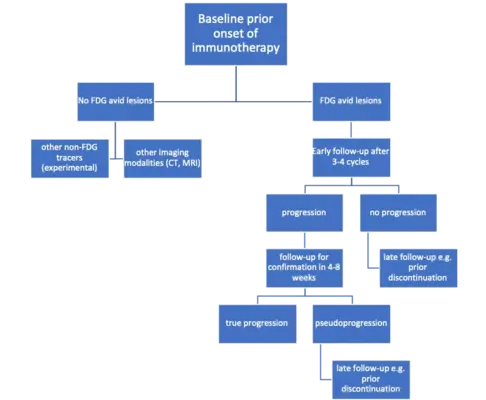
Abb. 1c. 18F-FDG PET-CT zur Überwachung der Immuntherapie (Dimitrakopoulou-Strauss A et al. Cancer Biother Radiopharm 2023; 38:225-231)
2. Longitudinale PET-CT-Studien mit FDG bei Patienten mit nicht resektablen Lungentumoren unter Immuntherapie oder kombinierter Chemo-Immuntherapie sowie bei resektablen Lungentumoren im neoadjuvanten Setting
Patienten mit metastasiertem NSCLC oder SCLC (Gruppe 1) und Patienten mit resektablem NSCLC (Gruppe 2) werden im Zeitverlauf mit dynamischem PET/CT und 18F-FDG untersucht. Gruppe 1 wird vor der Erstlinienbehandlung mit einem PD-1/PD-L1-Inhibitor als Monotherapie oder in Kombination mit Chemotherapie und in einer standardisierten Nachbeobachtung nach Therapiebeginn untersucht. Gruppe 2 wird vor Beginn der neoadjuvanten kombinierten Immun- und Chemotherapie und nach Abschluss der präoperativen Zyklen und nach Abschluss aller Therapien untersucht.
Ziel dieser Studie ist es, unter Berücksichtigung der klinischen Daten die Eignung von dynamischem PET/CT als frühes quantitatives Bildgebungsverfahren zur Erkennung von Progression/Reaktion zu beurteilen. Als Referenz dienen das progressionsfreie Überleben (PFS) und das Gesamtüberleben (OS) für beide Gruppen. In Gruppe 2 wird die pathologische Remission auch zur Bewertung des Ansprechens auf die neoadjuvante Therapie (pCR [d. h. 0 % lebensfähiges Tumorgewebe], MPR [d. h. < 10 % lebensfähiges Tumorgewebe]) herangezogen.
Kooperation mit Prof. Dr. med. Michael Thomas, Chefarzt der Abteilung Innere Medizin – Onkologie der Thoraxklinik Heidelberg.
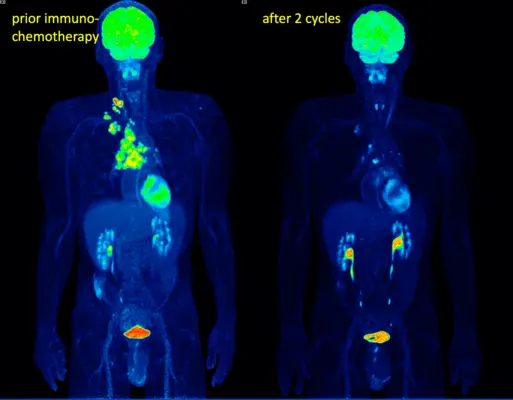
Abb. 2. Frühes Ansprechen nach 2 Zyklen kombinierter Immun- und Chemotherapie bei primärem nicht resektablem Lungenkrebs
3. Randomisierte multizentrische Phase III Studie zur Bewertung einer Induktionstherapie mit Lenalidomid, Bortezomib und Dexamethason mit entweder intravenös oder subkutan verabreichtem Isatuximab(GMMG HD-8-Studie)
Das Multiple Myelom zeigt in bildgebenden Verfahren häufig eine heterogene Beteiligung im Knochenmark und in extramedullären Herden. Bildgebende Verfahren wie die funktionelle Magnetresonanztomographie (MRT) und die Positronen-Emissions-Tomographie - Computertomographie (PET/CT) ermöglichen eine ergänzende nichtinvasive Diagnostik und geben Aufschluss über die Schädigung des mineralisierten Knochens, die Morphologie und die Pathophysiologie der Myelomzellen und ihrer Umgebung.
Die Ziele dieser Studie sind:
- Erfassung hochwertiger, vergleichbarer quantitativer Daten aus diffusionsgewichteten MRT- und PET/CT-Ganzkörperuntersuchungen zu Studienbeginn und im Verlauf
- Erkennung resistenter Läsionen während der Studientherapie
- Ermittlung der prognostischen Bedeutung von MRT und PET/CT bei PFS und OS, insbesondere im Vergleich zu parallelen Analysen der minimalen Resterkrankung (MRD) aus Beckenkammaspiraten.
Kooperation mit Prof. Dr. med. Hartmut Goldschmidt, Klinik für Innere Medizin V, Universitätsklinikum Heidelberg, Heidelberg, Deutschland; Nationales Centrum für Tumorerkrankungen Heidelberg, Heidelberg
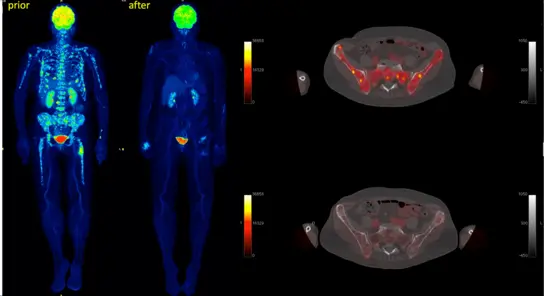
Abb. 3. Frühes Ansprechen nach Induktionschemotherapie bei multiplem Myelom (Sachpekidis C et al. Haematologica. 2019; 104:e420-e423)
4. Longitudinale PET-CT-Studien mit FDG bei Patienten mit Lymphomen unter CART-Zelltherapie
Die Car-T-Zelltherapie als neue zelluläre Immuntherapie bietet große Chancen für Patienten und stellt gleichzeitig neue Herausforderungen an die Bildgebung. Die FDG-PET/CT stellt den Goldstandard für die Bildgebung aggressiver Lymphome wie des großzelligen B-Zell-Lymphoms (DLBCL) dar und wurde daher auch als Standard in Studien zur Car-T-Zelltherapie eingesetzt. Die metabolische Beurteilung der Glukoseaufnahme mittels PET/CT ist der morphologischen Beurteilung mittels CT deutlich überlegen und wird daher fachübergreifend für das Staging und die Nachsorge des großzelligen B-Zell-Lymphoms empfohlen. Diagnostische Vorteile der MRT sind die bessere Beurteilung der Knochen- oder Knochenmarkinfiltration und die Unabhängigkeit vom Glukosestoffwechsel. Schließlich ermöglicht die fehlende Strahlenbelastung eine engmaschigere Therapieüberwachung.
Ziele der Studie sind:
- Evaluierung und Vergleich von PET/CT und Ganzkörper-MRT bei Patienten, die zur Therapiebeurteilung Car-T-Zellen erhalten
Kooperation mit Prof. Dr. med. Peter Dreger, Klinik für Innere Medizin V, Universitätsklinikum Heidelberg, Heidelberg, Deutschland; Nationales Centrum für Tumorerkrankungen Heidelberg, Heidelberg und der Radiologie des DKFZ
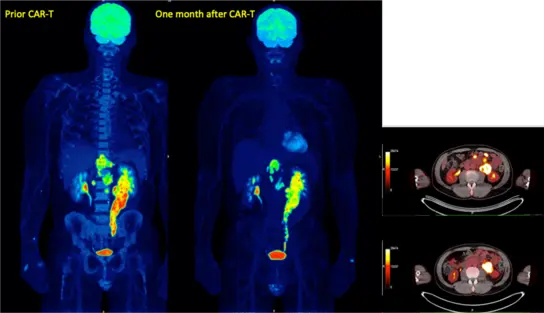
Abb. 4. Frühes Ansprechen ein Monat nach der CAR-T-Zelltherapie bei resistentem diffusem großzelligem B-Zell-Lymphom