Neuroblastome gehören zu den häufigsten Tumoren bei Kleinkindern und Säuglingen. Sie treten im Bereich der Nebennieren auf oder entlang der Wirbelsäule im Hals, Brustkorb oder Bauchbereich. Eine Besonderheit von Neuroblastomen ist ihr extrem unterschiedlicher Krankheitsverlauf: In einigen Fällen bildet sich der Tumor ohne jegliche Therapie komplett zurück. Bei etwa der Hälfte der Patienten kann jedoch auch eine hochintensive Therapie ein aggressives Wachstum nicht verhindern.
Es gibt derzeit jedoch kein international anerkanntes einheitliches Verfahren, um Hochrisikopatienten bereits bei der Erstdiagnose zuverlässig von denen mit einem günstigen Krankheitsverlauf zu unterscheiden.
„Bislang ging man davon aus, dass es sich dabei um ganz unterschiedliche Neuroblastom-Erkrankungen handelte“, sagt Thomas Höfer vom Deutschen Krebsforschungszentrum (DKFZ). Das Team um die Forschungsgruppenleiter Höfer und Frank Westermann vom Hopp-Kindertumorzentrum Heidelberg (KiTZ) und DKFZ konnte jetzt erstmals zeigen, dass sowohl Neuroblastome von Hochrisikopatienten, als auch jene mit einem günstigen Krankheitsverlauf einen gemeinsamen zellulären Ursprung haben. Bereits in der Embryonalentwicklung während des ersten Drittels der Schwangerschaft beginnt die Zellteilung aus dem Ruder zu laufen und schon da werden die Weichen für einen günstigen oder aggressiven Verlauf bei Kindern gestellt, zeigt die vorliegende Studie.
Die Wissenschaftlerinnen und Wissenschaftler entschlüsselten dafür das Tumorgenom von 100 Patientinnen und Patienten mit Neuroblastomen unterschiedlicher Stadien. Anschließend rekonstruierten sie anhand bestimmter Erbgutveränderungen die Entstehungsgeschichte der Tumoren. „Man geht davon aus, dass sich Erbgutveränderungen in unserem Genom zufällig und über die Zeit hinweg mit konstanter Geschwindigkeit wie Sand in einer Sanduhr anhäufen“, erklärt die Erstautorin der Studie Verena Körber aus der Arbeitsgruppe für theoretische Systembiologie von Thomas Höfer am DKFZ. „Das wird auch als molekulare Uhr bezeichnet und ist messbar. Mit Hilfe eines speziell dafür entwickelten mathematischen Modells konnten wir daraus einen Stammbaum der Neuroblastom-Entstehung rekonstruieren“, sagt Körber weiter.
Der Stammbaum zeigt, zu welchem Zeitpunkt die Krebszellen ganz unterschiedliche Entwicklungswege einschlagen und welche genetischen Ereignisse dafür entscheidend sind. Indem die Wissenschaftlerinnen und Wissenschaftler die Ergebnisse mit dem klinischen Verlauf korrelierten, ließen sich die Neuroblastome in zwei Kategorien einteilen: Solche, in denen genetische Veränderungen bereits früh zum Tumorwachstum führen. „Paradoxerweise sind das die Tumoren mit einem günstigen Verlauf, auch wenn sie zunächst schneller wachsen. Aber es finden keine drastischen genetischen Ereignisse mehr statt, die den Krebszellen das Rüstzeug geben, langfristig unsterblich zu werden“, erläutert Frank Westermann, Experte für kindliche Neuroblastome am KiTZ und DKFZ. „Außerdem werden sie aufgrund ihres frühen schnellen Wachstums in der Regel auch früher bei den Kindern erkannt.“
Bei der zweiten Kategorie handelt es sich um Neuroblastome, die erst später bösartig werden, dann aber aggressiv wachsen. Sie durchlaufen eine komplexere und langwierigere Evolution. Thomas Höfer sieht die Ursachen dafür darin, dass aufgrund der Zellumgebung oder interner genetischer Schäden die meisten dieser Neuroblastomzellen absterben: „Durch diesen Selektionsdruck entwickeln sie dann aber besonders aggressive Mechanismen, um dem Zelltod dauerhaft zu entgehen und unendlich teilungsaktiv zu bleiben. Bis es soweit ist, bleiben die Tumoren aber erst einmal klein und werden daher leider auch erst später diagnostiziert.“
An mathematischen Modellen der Krebsevolution wird derzeit auch in der Erwachsenenonkologie geforscht, um den Krankheitsverlauf beispielsweise bei Leukämien vorhersagen zu können.
Bei Kindern mit Neuroblastomen könnten sie helfen, junge Hochrisikopatienten von Kindern zu unterscheiden, die gar keine Therapie benötigen, so hofft das Forscherteam. „Wir arbeiten derzeit daran, die Tumorevolution als zuverlässigen Biomarker bei Neuroblastomen zu etablieren“, sagt Westermann. „Im Idealfall würde so eine Analyse nach der Probenentnahme dann nur etwa drei Wochen dauern, um eine individuelle Therapieempfehlung geben zu können.“
Originalpublikation:
Körber, V. et al. Neuroblastoma arises in early fetal development and its evolutionary duration predicts outcome. In: Nature Genetics (Online Publikation March 27, 2023) DOI: 10.1038/s41588-023-01332-y
Ein Bild zur Pressemitteilung steht zum Download zur Verfügung:
https://www.kitz-heidelberg.de/fileadmin/media/kitz/news/2023/230327-mitose_test-KiTZ.jpg
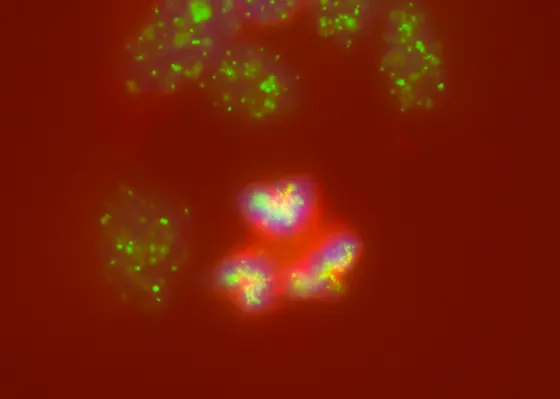
Bildunterschrift:
In Neuroblastomen läuft die Zellteilung aus dem Ruder: Statt Chromosomen (blau) gleichmäßig auf Tochterzellen aufzuteilen, bilden sich mehrere Spindelpole (grün) und Spindelapparate (rot), die sogar zum Zerbrechen von Chromosomen oder ihrer fehlerhaften Aufteilung führen.
Nutzungshinweis für Bildmaterial zu Pressemitteilungen
Die Nutzung ist kostenlos. Das Deutsche Krebsforschungszentrum (DKFZ) gestattet die einmalige Verwendung in Zusammenhang mit der Berichterstattung über das Thema der Pressemitteilung bzw. über das DKFZ allgemein. Bitte geben Sie als Bildnachweis an: „Quelle: Sina Kreth/KiTZ“.
Eine Weitergabe des Bildmaterials an Dritte ist nur nach vorheriger Rücksprache mit der DKFZ-Pressestelle (Tel. 06221 42 2854, E-Mail: presse@dkfz.de) gestattet. Eine Nutzung zu kommerziellen Zwecken ist untersagt.