Solange wir gesund sind, hält unser Körper die Anzahl an Blut- und Immunzellen weitestgehend konstant. Doch bei jedem Infekt oder anderen Störungen, die den Zellverbrauch erhöhen, kommt es zu Zellverlusten, die so rasch wie möglich wieder ersetzt werden müssen, um das Immunsystem voll funktionsfähig zu erhalten.
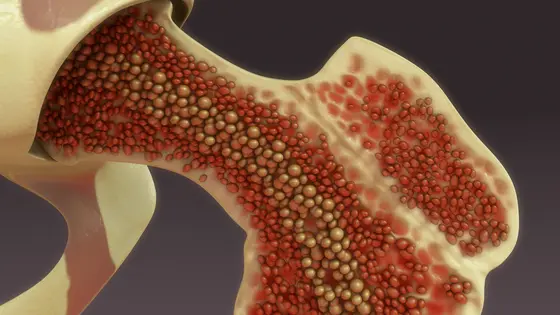
Während der Embryonalentwicklung bringen Blutstammzellen im Knochenmark alle Arten an reifen Blutzellen hervor. „Daher wurde lange vermutet, dass der Verlust an Blut- und Immunzellen in Notfallsituationen an die Blutstammzellen signalisiert wird, die dadurch angeregt werden, sich deutlich schneller als sonst zu teilen, um umgehend für Ersatz zu sorgen“, sagt Hans-Reimer Rodewald vom DKFZ.
Blutstammzellen können sich in eine Tochterzelle teilen, die Stammzelle bleibt, und in eine zweite Tochterzelle, die sich weiterentwickelt. Aus diesen sich weiterentwickelnden Tochterzellen entstehen zunächst die sogenannten multipotenten Vorläuferzellen, die in der Lage sind, zu jeder Art von Blutzellen heranzureifen. „Bis heute wussten wir nicht genau, ob im Notfall tatsächlich die Blutstammzellen für Regeneration sorgen – oder ob die Vorläuferzellen diesen Job übernehmen“, erklärt die Immunologin Katrin Busch, eine der Erstautorinnen der aktuellen Arbeit.
An Mäusen konnte das Team um Rodewald, in Zusammenarbeit mit dem Team um Thomas Höfer, ebenfalls DKFZ, diese Frage nun untersuchen. Dazu nutzen die Forscher genetische Markierungen, die in die Blutstammzellen eingebaut wurden und die sich über alle weiteren Entwicklungsschritte in deren Zell-Nachkommenschaft nachverfolgen lassen.
Erkrankten die Mäuse an einem bakteriellen Infekt, so entwickelten sie eine systemische Entzündung. Darauf reagierten die markierten Blutstammzellen zwar wie erwartet mit Zellteilung – doch daraus resultierte keine erhöhte Zahl an differenzierten Blutzellen. Außerdem intensivierten die Stammzellen die Transkription, also das Ablesen von Genen – doch dies betraf in erster Linie solche Erbanlagen, die mit der Selbsterhaltung der Stammzellen in Verbindung stehen. Die Blutstammzellen selbst sind also offenbar nicht die Nachschublieferanten von reifen Blutzellen. Auch in anderen gesundheitlichen Stress-Situationen, etwa bei einer Anämie oder bei einem Mangel verschiedener Arten von Immunzellen, bot sich den Forschern das gleiche Bild.
Ganz anders sah es jedoch aus, wenn die Population der multipotenten Vorläuferzellen mit dem genetischen Marker ausgestattet wurde: Nach etwa elf Tagen stieg die Zahl verschiedener markierter weißer Blutkörperchen, die aus den multipotenten Vorläuferzellen hervorgingen, in den bakteriell infizierten Mäusen deutlich an.
„Dass die Vorläuferzellen diese Aufgabe übernehmen, hat mehrere Vorteile: Es beschleunigt den Prozess, denn die Differenzierung aus Stammzellen ist ein ziemlich langsamer Vorgang. Außerdem gibt es deutlich mehr Vorläuferzellen als Stammzellen – auch das trägt dazu bei, dass rasch genügend reife Blutzellen verfügbar sind“, erklärt Höfer. Rodewald ergänzt: „Wir deuten das Ergebnis außerdem als einen möglichen Schutzmechanismus der Blutstammzellen, vielleicht, um sich nicht im Laufe des Lebens durch immer wieder auftretende Infektionen zu verausgaben.“
Bereits vor einigen Jahren hatten Wissenschaftlerinnen und Wissenschaftler aus Rodewalds und Höfers Labor nachgewiesen, dass die pluripotenten Vorläuferzellen entgegen der gängigen Expertenmeinung auch bei der Aufrechterhaltung der Zahl der Blutzellen unter gesunden Normalbedingungen den Hauptanteil tragen.
Ann-Kathrin Fanti, Katrin Busch, Alessandro Greco, Xi Wang, Branko Cirovic, Fuwei Shang, Tamar Nizharadze, Larissa Frank, Melania Barile, Thorsten Feyerabend, Thomas Hofer, and Hans-Reimer Rodewald: Flt3- and Tie2-Cre tracing identifies regeneration in sepsis from multipotent progenitors but not hematopoietic stem cells
Cell Stem Cell 2023, DOI: doi.org/10.1016/j.stem.2022.12.014