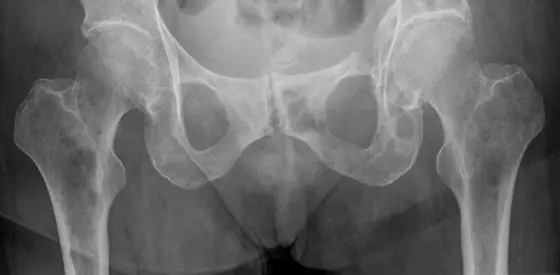
Knochen erscheinen als beständig und solide. Doch der Schein trügt: Tatsächlich ist das Knochengewebe im stetigem Umbau. Knochenabbauende Osteoklasten und knochenaufbauende Osteoblasten sorgen im gesunden Organismus für ein fein austariertes Gleichgewicht.
Doch diese Balance ist gelegentlich gestört: Bei der Osteoporose nimmt der Knochenabbau überhand, so dass es zu Brüchen und Deformationen kommen kann. Auch bei der Entstehung von Knochenmetastasen, die im Verlauf vieler Krebserkrankungen auftreten, nehmen häufig knochenabbauende Prozesse überhand. Das gilt auch für das Multiple Myelom, das im Knochenmark entsteht und sich dort ausbreitet.
„Einmal in den Knochen vorgedrungen, sondern viele Krebszellen Substanzen ab, die den Knochenaufbau durch die Osteoblasten unterdrücken. Die Patienten leiden oft sehr unter den schmerzenden Knochenmetastasen und es kommt häufig zu Brüchen“, sagt Sonja Loges vom DKFZ-Hector-Krebsinstitut an der Universitätsmedizin Mannheim*.
Bislang stehen Medikamente zur Verfügung, die den Knochenabbau durch Osteoklasten hemmen. Loges und ihre Mitarbeiterin Isabel Ben Batalla halten aber auch Wirkstoffe, die den Knochenaufbau durch die Osteoblasten fördern, für medizinisch erforderlich. Um solche Substanzen zu identifizieren, mussten die Forscherinnen zunächst herausfinden, welche Signalwege die Aktivität der Osteoblasten steuern.
Bei dieser Untersuchung identifizierte das Team in Mäuse-Osteoblasten die beiden Enzyme MERTK und Typo3, so genannte Rezeptor-Tyrosinkinasen, die die Knochenproduktion regulieren. Die Funktion der beiden Enzyme wurde an Mäusen untersucht, in deren Osteoblasten entweder die eine oder die andere Rezeptor-Tyrosinkinase genetisch ausgeschaltet war. Das Ergebnis: War MERTK inaktiviert, so nahm die Knochenmasse der Tiere zu. Ohne Typo3 dagegen nahm sie ab.
Dieses Ergebnis war ein Hinweis darauf, dass die Aktivität von MERTK in Osteoblasten auch zur krebsbedingten Hemmung der Knochenbildung beitragen könnte.
MERTK-Inhibitor kurbelt Knochenbildung an
Der niedermolekulare Wirkstoff R992 hemmt die Aktivität von MERTK. „Damit hatten wir ein Werkzeug in der Hand um zu prüfen, ob eine Hemmung von MERTK den krebsbedingten Knochenabbau bremsen kann“, sagt Janik Engelmann, Erstautor der Studie vom Universitätsklinikum Hamburg-Eppendorf und dem DKFZ-Hector Krebsinstitut. Wurden gesunde Mäuse mit R992 behandelt, so stieg die Zahl ihrer Osteoblasten und die Knochenmasse der Tiere nahm zu. Auch in Mausmodellen mit Myelom-, Lungenkrebs- und Brustkrebs-Zelllinien reduzierte die Behandlung mit R992 den Knochenschwund sowie die Anzahl der Knochenmetastasen.
Der Wirkstoff R992 ist nicht als Medikament zugelassen. Um die Effekte einer MERTK-Blockade möglicherweise auch an Patientinnen und Patienten untersuchen zu können, entwickelt das Team um Sonja Loges am Deutschen Krebsforschungszentrum derzeit einen Antikörper, der gezielt die Funktion von MERTK blockiert. „Knochenmetastasen betreffen sehr viele Krebspatienten. Die Osteoporose ist ebenfalls eine häufige Erkrankung. Ein Medikament, das dem unheilvollen Knochenschwund entgegenwirkt, könnte daher sehr vielen Erkrankten zugutekommen. Daher investieren wir in die weitere Erforschung der Rolle von MERTK als therapeutisches Ziel beim krankhaften Knochenabbau.“
* Das DKFZ-Hector-Krebszentrum an der Universitätsmedizin Mannheim ist eine Kooperation des Deutschen Krebsforschungszentrums (DKFZ), der Medizinischen Fakultät Mannheim der Universität Heidelberg und des Universitätsklinikums Mannheim.
Janik Engelmann, Jennifer Zarrer, Victoria Gensch, Kristoffer Riecken, Nikolaus Berenbrok, The Vinh Luu, Antonia Beitzen-Heineke, Maria Elena Vargas-Delgado, Klaus Pantel, Carsten Bokemeyer, Somasekhar Bhamidipati, Ihab S. Darwish, Esteban Masuda, Tal Burstyn-Cohen, Emily J. Alberto, Sourav Ghosh, Carla Rothlin, Eric Hesse, Hanna Taipaleenmäki, Isabel Ben-Batalla, Sonja Loges: Regulation of bone homeostasis by Mertk and TYRO3
Nature Communications 2022 Dec 12;13(1):7689., DOI: 10.1038/s41467-022-33938-x