Ein ausbalancierter Eisen-Stoffwechsel ist eine wesentliche Voraussetzung für unsere Gesundheit. Dass Eisenmangel zu Blutarmut führt, gehört fast schon zum Allgemeinwissen: Das Metall ist wichtiger Bestandteil des Blutfarbstoffs Hämoglobin, der in den roten Blutkörperchen für den Sauerstoff-Transport verantwortlich ist. Gleichermaßen fatal ist ein Überschuss an Eisen, der zur Entstehung schädlicher Sauerstoff-Radikale führen kann.
Die Eisenversorgung der Zellen wird von den beiden Proteinen IRP-1 und IRP-2 gesteuert. Fehlt es der Zelle an Eisen, so kurbeln IRP-1 und IRP-2 die Produktion der verschiedenen Eisentransporter-Proteine an, die Eisen in die Zelle aufnehmen. IRP-1 und IRP-2 sorgen ebenfalls dafür, dass es nicht zu einem ebenso gefährlichen Eisen-Überschuss kommt.
IRP-1 und IRP-2 sind überlebenswichtig: Mäuse, denen beide Steuerproteine während der Embryonalentwicklung fehlen, sterben noch im Mutterleib. Doch was passiert, wenn bei erwachsenen Mäusen IRP-1 und IRP-2 ausfallen? Ein Team um Bruno Galy am DKFZ hat dies nun an Mäusen untersucht, deren IRP-Produktion im gesamten Körper durch die Injektion eines Wirkstoffs abgeschaltet werden kann.
Wie die Forscher erwartet hatten, war die auffälligste Veränderung nach Abschalten der IRPs ein ausgeprägter Rückgang der roten Blutkörperchen, die außerdem aufgrund des Hämoglobin-Mangels nur ein Miniaturformat erreichten.
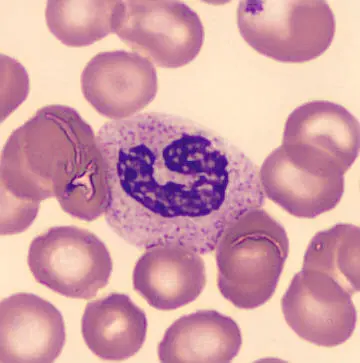
Überrascht war das Team jedoch darüber, dass auch die Zahl der weißen Blutkörperchen extrem zurückging. Bei näherer Untersuchung stellte sich heraus, dass dieser Rückgang hauptsächlich einem Mangel an neutrophilen Granulozyten geschuldet war. Diese auch kurz als „Neutrophile“ bezeichneten Immunzellen machen beim Menschen bis zu zwei Drittel der weißen Blutkörperchen aus und sind wichtiger Bestandteil der angeborenen Immunabwehr.
Dieser Rückgang wird nicht durch ein Massensterben der Neutrophilen verursacht, sondern durch eine Entwicklungsblockade im blutbildenden System: Die Vorläuferzellen im Knochenmark entwickeln sich nicht mehr zu reifen Neutrophilen, da der Differenzierungsprozess eisenabhängig ist. Andere weiße Blutkörperchen, etwa die Monozyten, waren nicht von der IRP-abhängigen Entwicklungsblockade betroffen.
Eisenmangel als zweischneidiges Schwert
„Diese starke Eisen-Abhängigkeit der Granulozyten-Differenzierung war bislang unbekannt und könnte sich auch auf die Immunabwehr von bakteriellen Krankheitserregern auswirken“, vermutet Studienleiter Bruno Galy. Interessanterweise ist Eisenmangel eine bekannte Verteidigungsstrategie des Körpers bei bakteriellen Infekten: Viele Krankheitserreger sind abhängig von Eisen. Um ihre Vermehrung zu bremsen, hortet der Körper das Metall in bestimmten Zellen, die als Vorratskammer dienen. So erschwert er den Erregern den Zugriff auf die wertvolle Ressource.
Tatsächlich bestätigt eine weitere Publikation* in der gleichen Ausgabe der Zeitschrift „Science Advances“ Galys Vermutung: Eisenmangel im Blutserum, wie er typischerweise bei Infektionen auftritt, führt bei Mäusen zu einem Rückgang der Neutrophilen und schränkt ihre Fähigkeit ein, Bakterien zu bekämpfen, zeigen die Autoren der Studie, an der Bruno Galy ebenfalls beteiligt ist.
„An den Mäusen konnten wir beobachten, dass Eisenmangel offenbar das angeborene Immunsystem moduliert. Er unterdrückt die Granulozytenreifung und drosselt außerdem die Abwehrkraft der Neutrophilen“, sagt Bruno Galy und ergänzt: „Die Limitierung des verfügbaren Eisens ist ein zweischneidiges Schwert: Einerseits verhindert der Körper dadurch die Ausbreitung von Bakterien. Anderseits leidet darunter die Funktion eines wichtigen Arms des angeborenen Immunsystems.“
Nicht nur Infektionen, sondern auch Entzündungen führen oft zu Eisenmangel und damit zu einer Anämie. Krebspatienten, deren Erkrankung mit chronisch-entzündlichen Veränderungen einhergeht, sind daher oft von Blutarmut betroffen, was ihre Lebensqualität stark einschränken kann. „Als Nächstes wollen wir klären, ob auch der Eisenmangel bei chronischen Entzündungen die Funktion der Immunabwehr beeinträchtigt“, erklärt Galy.
Michael Bonadonna, Sandro Altamura Elisabeth Tybl, Gael Palais, Maria Qatato, Maria Polycarpou-Schwarz, Martin Schneider, Christina Kalk, Wibke Rüdiger, Alina Ertl, Natasha Anstee, Ruzhica Bogeska, Dominic Helm, Michael D. Milsom, Bruno Galy: Iron regulatory protein (IRP-)mediated iron homeostasis is critical for neutrophil development and differentiation in the bone marrow.
Science Advances 2022, DOI: https://doi.org/10.1126/sciadv.abq4469
* Joe N. Frost, Sarah K. Wideman, Alexandra E. Preston, Megan R Teh, Zhichao Ai, Lihui Wang, Amy Cross, Natasha White, Yavuz Yazicioglu, Michael Bonadonna, Alexander J. Clarke, Andrew E. Armitage, Bruno Galy, Irina A. Udalova, Hal Drakesmith: Plasma iron controls neutrophil production and function
Science Advances 2022, DOI: https://doi.org/10.1126/sciadv.abq5384