Auch Tumoren, die zunächst gut auf eine Behandlung ansprechen, nehmen oft ihr Wachstum wieder auf oder breiten sich sogar über Metastasen im ganzen Körper aus. Die Ursache dafür ist, dass sich Krebszellen beim Fortschreiten der Erkrankung stetig weiterentwickeln. Sie durchlaufen regelrecht eine Evolution, in deren Verlauf sie sich in voneinander abweichende Zellklone differenzieren, die neue biologische Eigenschaften erlangen. „Diese neu erworbenen molekularen Merkmale erlauben den Krebszellen sehr häufig, der Wirkung von zunächst wirksamen Medikamenten zu entkommen. Die Therapieresistenz ist die gefährlichste Begleiterscheinung der Tumorevolution“, erklärt Jens Siveke vom Deutschen Konsortium für Translationale Krebsforschung und vom Westdeutschen Tumorzentrum des Universitätsklinikums Essen.
Siveke ist der Koordinator des neuen interdisziplinären Forschungsnetzwerks SATURN3, das den biologischen Hintergründen der Therapieresistenzen auf den Grund gehen will, die als Konsequenz der Heterogenität von Tumorzellen entstehen. Insgesamt 13 Forschungseinrichtungen sind an SATURN3 beteiligt.
Das BMBF hat im Rahmen der Nationalen Dekade gegen Krebs eine neue Förderrichtlinie eingerichtet, die erfolgversprechenden wissenschaftlichen Kooperationsprojekten ermöglichen soll, diese Zusammenhänge zu erforschen und damit zu besseren Behandlungsoptionen für therapieresistente Tumoren beizutragen. SATURN3 wurde nun als eines von zwei Projekten zur Förderung ausgewählt.
„Damit trägt das BMBF zur Klärung einer der großen ungelösten Fragen der Krebsforschung bei“, sagt Michael Baumann, Vorstandsvorsitzender des DKFZ und Ko-Vorsitzender im Strategiekreis der Nationalen Dekade gegen Krebs. „Die hochkarätigen Konsortien, die nun ihre Arbeit aufnehmen können, haben gute Aussichten, mit ihren Ergebnissen die Krebsmedizin entscheidend voranzubringen.“
Die im Projekt SATURN3 vernetzten Wissenschaftlerinnen und Wissenschaftler konzentrieren sich auf drei Krebsarten, die heute noch sehr schwierig zu behandeln sind – und die sehr viele Menschen betreffen: Darmkrebs, Krebs der Bauchspeicheldrüse sowie zwei besonders aggressive Formen von Brustkrebs (Triple-negativ und Luminal B).
Das Besondere am Konzept von SATURN3 ist, dass den Patientinnen und Patienten nicht nur bei der Erstdiagnose Tumorbiopsien entnommen werden, sondern dass im Verlauf der Erkrankung mehrfach Gewebeproben der Tumoren gewonnen werden. So erhalten die Forschenden auch Tumorzellen, die bereits Resistenzen entwickelt haben.
Das Tumormaterial wird dann genetisch, epigenetisch und funktionell untersucht, und zwar für jede einzelne Zelle separat, um die extreme Heterogenität der Tumoren darzustellen. Dabei können die beteiligten Forschungsteams auf modernste analytische Techniken, bildgebende Verfahren sowie Methoden der künstlichen Intelligenz zugreifen, die bei den Partnerinstitutionen des Konsortiums etabliert sind.
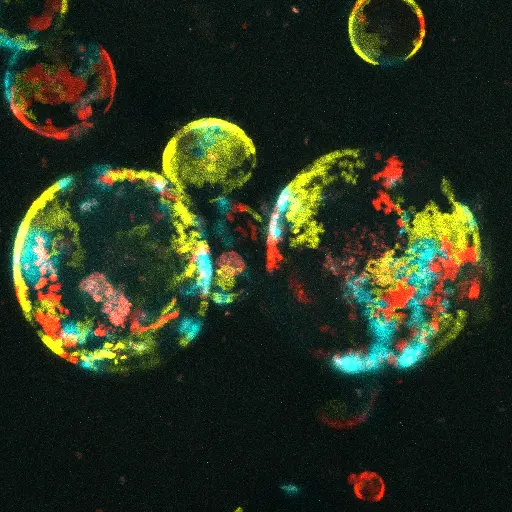
„So machen wir uns für jeden Patienten ein zeitaufgelöstes, mehrdimensionales Bild der Tumoren auf Einzelzell-Ebene. Dabei können wir erkennen, mit welchen molekularen Anpassungen sich die Krebszellen den jeweiligen Therapien entziehen. Ist dieser Prozess verstanden, können wir ihn möglicherweise gezielt blockieren“, erklärt Andreas Trumpp vom DKFZ und HI-STEM, Ko-Koordinator von SATURN3. „An Tumor-Organoiden, die in der Kulturschale aus dem Tumormaterial gezüchtet werden, werden wir die neuen therapeutischen Ansätze zur Resistenzüberwindung erproben und dann in einem weiteren Validierungsschritt in Tiermodellen prüfen.“
Wilko Weichert von der Technischen Universität München und ebenfalls Ko-Koordinator von SATURN3, erklärt: „Letztendlich ist unser Ziel, molekulare Veränderungen der Krebszellen zu identifizieren, die als zuverlässige Biomarker auf eine entstehende Resistenz hinweisen. In frühen klinischen Studien wird dann geprüft, ob sich diese mit neuen zielgerichteten Medikamenten oder Wirkstoffkombinationen überwinden lassen.“ Zum SATURN3-Konsortium zählen daher auch Arbeitsgruppen, die große Expertise in der Entwicklung von klinischen Studienprotokollen haben. SATURN3 wird außerdem beraten und unterstützt durch Patientenvertreterinnen und -vertreter, die ihre Erfahrungen direkt in den Forschungsprozess einbringen.
„Die aus der Heterogenität entstehenden Therapieresistenzen sind ein immenses medizinisches Problem. Je genauer wir diese Vorgänge im Tumor verstehen, desto besser können wir Strategien entwickeln, die verhindern, dass Krebstherapien ihre Wirksamkeit verlieren“, fasst Studienkoordinator Jens Siveke die Ziele von SATURN3 zusammen.
* SATURN3: Spatial and Temporal Resolution of Intratumoral Heterogeneity in 3 hard-to-treat Cancers
** HI-STEM: Das Heidelberg Institute for Stem Cell Technology and Experimental (HI-STEM) gGmbH wurde 2008 als Public-Private-Partnership von DKFZ und Dietmar Hopp Stiftung gegründet
An SATURN3 beteiligte Institutionen (alphabetisch):
- Deutsches Konsortium für translationale Krebsforschung (DKTK)
- Deutsches Krebsforschungszentrum (DKFZ)
- European Molecular Biology Laboratory (EMBL), Heidelberg
- Georg Speyer Haus Frankfurt
- German Breast Group
- HI-STEM gGmbH
- LMU Klinikum München
- Universitätsklinikum Augsburg
- Universitätsklinikum Essen
- Universitätsklinikum Frankfurt
- Universitätsklinikum Freiburg
- Universitätsklinikum Göttingen
- Universitätsklinikum Heidelberg
- Universitätsklinikum Köln
- Universitätsklinikum Marburg
- Universitätsklinikum Regensburg
- Technische Universität München (TUM) mit ihrem Universitätsklinikum rechts der Isar
Ein Bild zur Meldung steht zum Download zur Verfügung unter:
OrganoideforSaturn3.jpg
BU: Aus einzelnen Tumorzellen können zu verschiedenen Zeitpunkten der Erkrankung in der Kulturschale „Minitumoren“, so genannte Tumororganoide gezüchtet werden. Daran lässt sich die Evolution der Krebszellen beobachten und ihre Reaktion auf Wirkstoffe testen.
Nutzungshinweis für Bildmaterial zu Pressemitteilungen
Die Nutzung ist kostenlos. Das Deutsche Krebsforschungszentrum (DKFZ) gestattet die einmalige Verwendung in Zusammenhang mit der Berichterstattung über das Thema der Pressemitteilung bzw. über das DKFZ allgemein. Bitte geben Sie als Bildnachweis an: „Quelle: Jackstadt/HI-STEM
Eine Weitergabe des Bildmaterials an Dritte ist nur nach vorheriger Rücksprache mit der DKFZ-Pressestelle (Tel. 06221 42 2854, E-Mail: presse@dkfz.de) gestattet. Eine Nutzung zu kommerziellen Zwecken ist untersagt.
Im Deutschen Konsortium für Translationale Krebsforschung (DKTK) verbindet sich das Deutsche Krebsforschungszentrum (DKFZ) in Heidelberg als Kernzentrum langfristig mit onkologisch besonders ausgewiesenen universitären Partnerstandorten in Deutschland.