Hirnmetastasen sind eine gefürchtete Komplikation fortgeschrittener Krebserkrankungen. Die verschiedenen Krebsarten unterscheiden sich in ihrer Tendenz, das Gehirn zu besiedeln. Schwarzer Hautkrebs in fortgeschrittenen Stadien bildet in fast der Hälfte aller Fälle Absiedlungen im Gehirn, auch bei bestimmten Formen von Brustkrebs und Lungenkrebs treten Hirnmetastasen sehr häufig auf.
Hirnmetastasen sind häufig nicht operativ zu entfernen und sprechen oft nicht langfristig auf Behandlungen an. „Bei Krebsarten, die sehr häufig ins Gehirn streuen, wäre den Betroffenen extrem geholfen, wenn wir eine präventive Behandlung zur Verfügung hätten, die verhindern kann, dass Hirnmetastasen entstehen“, erklärt Frank Winker, Arbeitsgruppenleiter im Deutschen Krebsforschungszentrum sowie Geschäftsführender Oberarzt an der neurologischen Universitätsklinik Heidelberg.
Aus Beobachtungsstudien war bereits bekannt, dass antithrombotische Medikamente, die die Blutgerinnung hemmen, sich günstig auf die Prognose bestimmter Krebserkrankungen auswirken können. Möglicherweise beeinflussen diese Wirkstoffe die Metastasierung. Ob dies auch für Hirnmetastasen gilt und wenn ja, auf welche Weise hier Blutgerinnung und Metastasierung zusammenhängen, untersuchten Winkler und seine Kollegen nun an Mäusen. Dazu nutzen die Forscher eine spezielle mikroskopische Technik (in vivo multiphoton laser-scanning microscopy), die ihnen einen tiefen Blick in das Hirngewebe erlaubt und ermöglicht, einzelne Krebszellen zu verfolgen.
Die Mäuse erhielten Melanom- oder Brustkrebszellen in die Blutbahn gespritzt. Einzelne der zirkulierenden Tumorzellen setzten sich daraufhin in den feinen Blutkapillaren des Gehirns fest. Nur, wenn es diesen Zellen nun gelingt, durch die Gefäßwand ins Hirngewebe vorzudringen, können sie zur Hirnmetastase auswachsen. Winker und Kollegen beobachteten, dass sich um die festgesetzten Tumorzellen häufig Blutgerinnsel – wissenschaftlich: Thromben – bildeten. Krebszellen, um die sich kein solches Gerinnsel bildete, schafften es nicht, die Kapillarwand zu durchdringen. „Offenbar hilft der Thrombus den Zellen dabei, sich lange in der Kapillare festzuhalten, um die Passage durch die Gefäßwand vorbereiten zu können“, erklärt Winkler.
Die Heidelberger Forscher fanden heraus, dass die Tumorzellen offenbar direkt in die komplexe Kaskade der Blutgerinnung eingreifen und so die Entstehung der Thromben aktiv auslösen. Sie fördern die Entstehung des Gerinnungsfaktors Thrombin, der für die Bildung des langfaserigen Proteins Fibrin erforderlich ist, aus dem das Netzwerk des Gerinnsels hauptsächlich besteht.
Die Thrombus-Bildung, so erkannten die Forscher, ist für Tumorzellen die notwendige Voraussetzung, um die Kapillare zu verlassen und damit den entscheidenden ersten Schritt zur Bildung einer Hirnmetastase zu gehen. Ein Wirkstoff, der Thrombin hemmt, müsste also in der Konsequenz die Metastasierung unterdrücken, weil er die Tumorzellen daran hindert, ins Hirngewebe vorzudringen. Und tatsächlich: Mäuse, die den bereits als Medikament zugelassenen Thrombin-Hemmstoff Dabigatran erhielten, entwickelten signifikant weniger Metastasen als unbehandelte Tiere.
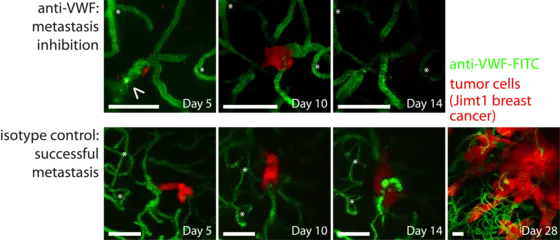
Auch die Hemmung eines weiteren Blutgerinnungsfaktors (von Willebrand-Faktor) mit spezifischen Antikörpern reduzierte bei den Mäusen die Bildung von Thromben – und in der Folge auch die Anzahl der entstehenden Hirnmetastasen.
„Wir konnten mit dieser Arbeit zeigen, dass vor allem der Einfluss der Krebszellen auf die plasmatischen Gerinnungsfaktoren die Entstehung von Hirnmetastasen begünstigt. Deshalb sollte ein präventives Medikament genau hier ansetzten.“, erklärt Manuel Feinauer, Erstautor der aktuellen Publikation.
„Unser Ziel ist es, Wirkstoffe zur Prävention von Hirnmetastasen bei Hochrisikopatienten zu identifizieren“, sagt Winkler. „Die Untersuchungen an Mäusen ist ein erster Schritt, um genau zu verstehen, auf welche Weise die Substanz die Besiedlung des Gehirns durch Tumorzellen verhindern kann. Langfristig wollen wir diese Wirkstoffe dann in klinischen Studien testen. Dazu müssen wir zunächst noch besser verstehen, für welche Krebs-Unterarten dieser Mechanismus besonders wichtig ist, und auch, ob wir Patienten mit einem besonders hohen Risiko für Gehirnmetastasen noch besser identifizieren können.“
Die Forscher sind optimistisch, denn Wirkstoffe, die Thrombin hemmen, haben zumindest einen bereits bekannten Vorteil: Sie werden seit längerem schon zur Prävention von Schlaganfällen verordnet und gelten daher als vergleichsweise gut verträglich, auch über lange Zeiträume.
Manuel J. Feinauer, Stefan Werner Schneider, Anna S. Berghoff, Jose Ramon Robador, Cedric Tehranian, Matthia A. Karreman, Varun Venkataramani, Gergely Solecki, Julia Katharina Grosch, Katharina Gunkel, Bogdana Kovalchuk, Frank Thomas Mayer, Manuel Fischer, Michael O. Breckwoldt, Maik Brune, Yannick Schwab, Wolfgang Wick, Alexander Thomas Bauer and Frank Winkler: Local blood coagulation drives cancer cell arrest and brain metastasis in a mouse model
Blood 2020, DOI: 10.1182/blood.2020005710