Wissenschaftlern der Medizinischen Fakultät Mannheim der Universität Heidelberg, unter der Leitung von Professor Dr. Adelheid Cerwenka, und des Deutschen Krebsforschungszentrums, unter der Leitung von Professor Dr. Thomas Höfer, ist es jetzt gelungen, ein Schlüsselmolekül zu identifizieren, das die Aktivität der Natürlichen Killerzellen bei der Tumorabwehr bremst. Diese Bremse zu lösen könnte eine vielversprechende Strategie sein, um NK-Zell-basierte Immuntherapien gegen solide Tumore zu verbessern.
Hypoxie ist ein häufiges Merkmal solider Tumoren. Die Zellen reagieren auf den Sauerstoffmangel, indem sie den Hypoxie Induzierten Transkriptionsfaktor-1α (HIF-1α) hochregulieren. Durch das spezifische Ausschalten dieses Moleküls in NK-Zellen konnte die Aktivität der Killerzellen stark erhöht und die Tumore in ihrem Wachstum im Mausmodell verlangsamt werden.
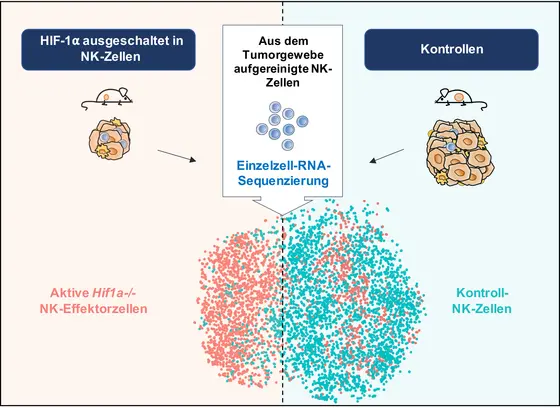
Einzelzell-RNA-Sequenzierung der in den Tumor eingewanderten NK-Zellen zeigte, dass in NK-Zellen ohne HIF-1α eine ganze Kaskade von gegen den Tumor wirksamen Faktoren ausgelöst wird. Die Hemmung von HIF-1α setzt offenbar eine gegen den Tumor gerichtete Aktivität der NK-Zellen frei, die für die Krebstherapie genutzt werden könnte.
Professor Dr. Adelheid Cerwenka erforscht am „Mannheim Institute for Innate Immunoscience“ (MI3) der Medizinischen Fakultät Mannheim NK-Zell-basierte Therapien gegen Krebs. „Der Grund dafür, dass NK-Zellen rasch ihre Angriffslust verlieren, sobald sie in das Tumorgewebe eingewandert sind, ist der Sauerstoffmangel in soliden Tumoren. Wenn es uns gelingt, diesen Bremsmechanismus auszuhebeln, können die Killerzellen ihr volles Potenzial im Kampf gegen den Tumor entfalten.“
Aus dem Transkriptionsmuster einzelner NK-Zellen erkannten die Wissenschaftler, dass ein Ausschalten von HIF-1α zu einer erhöhten Expression von Aktivierungsmarkern und Effektormolekülen und einer verstärkten Aktivierung des NF-κB Signalwegs führte. NF-κB ist ein wichtiger Transkriptionsfaktor, der die gegen den Tumor gerichteten Aktivität von Immunzellen maßgeblich steuert.
Nicht nur kultivierte NK-Zellen der Maus, sondern auch solche des Menschen zeigten eine erhöhte, gegen den Tumor gerichtete Reaktivität, wenn HIF-1α ausgeschaltet oder gehemmt wurde. Darüber hinaus konnten die Wissenschaftler zeigen, dass diese Aktivität vom Vorhandensein von Interleukin 18, einem körpereigenen Regulator-Protein des Immunsystems, abhing.
„Unsere Studie zeigt, dass der Transkriptionsfaktor HIF-1α als Immunkontrollpunkt fungiert, der die Natürlichen Killerzellen im Mikromilieu des Tumors hemmt. Auf diesen Ergebnissen aufbauend untersuchen wir nun in menschlichen NK-Zellen, ob wir die Ausschaltung von HIF-1α für eine therapeutische Anwendung nutzen können“, skizziert Dr. Ana Stojanovic, eine der Erstautorinnen der aktuell im renommierten Fachjournal Cell Immunity erschienen Arbeit, das weitere Vorgehen.
Publikation
Single-Cell RNA Sequencing of Tumor-Infiltrating NK Cells Reveals that Inhibition of Transcription factor HIF-1a unleashes NK cell activity
Jing Ni, Xi Wang, Ana Stojanovic, Qin Zhang, Marian Wincher, Lea Bühler, Annette Arnold, Margareta P. Correia, Manuel Winkler, Philipp-Sebastian Koch, Veronika Sexl, Thomas Höfer und Adelheid Cerwenka
Immunity (2020)
DOI: 10.1016/j.immuni.2020.05.001
(https.//doi.org/10.1016/j.immuni.2020.05.001)