Mit dem Ziel, den Nachweis des Krebsproteins p16 als diagnostischen Test zur Früherkennung von Gebärmutterhalskrebs zu entwickeln, hatten Wissenschaftler um Magnus von Knebel Doeberitz vom Deutschen Krebsforschungszentrum (DKFZ) und vom Universitätsklinikum Heidelberg 1999 das Unternehmen mtm laboratories („molecular tools in medicine“) gegründet. Die Firma war eine der ersten Ausgründungen, an der das DKFZ Anteile hielt.
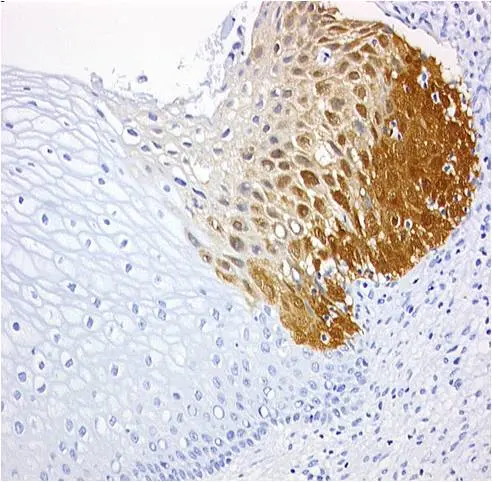
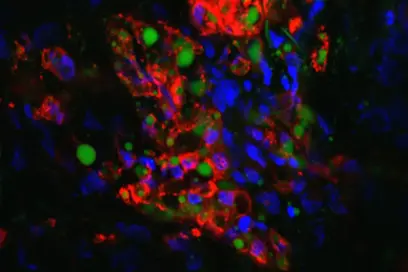
Das Unternehmen entwickelte den Test und brachte ihn unter dem Namen CINtec PLUS auf den Markt. Das immunhistologische Verfahren weist das gleichzeitige Vorhandensein der beiden Biomarker p16 und Ki-67 in einer einzigen Zelle nach. Ein positives Ergebnis signalisiert, dass eine HPV-infizierte Frau schon eine Krebsvorstufe entwickelt hat, die der sofortigen klinischen Abklärung bedarf. HPV-positive Frauen dagegen, bei denen der Test negativ ausfällt, haben keine Krebsvorstufe entwickelt, daher können die weiteren Vorsorgeintervalle wesentlich verlängert werden.
2011 wurde mtm laboratories von Roche übernommen, einem international führenden Anbieter von Diagnostika und Therapeutika. Roche erhielt nun die Zulassung der US-amerikanischen FDA (Food and Drug Administration) für CINtec PLUS zur Unterstützung von Klinikern bei der Verbesserung der Prävention von Gebärmutterhalskrebs. FDA-Zulassungen beruhen auf sehr aufwändigen Studien an vielen Tausenden Teilnehmern, bislang gibt es nur wenige Beispiele von Produkten deutscher Biotechunternehmen, die diese Hürde genommen haben. Es wird erwartet, dass der Test im Laufe des Jahres 2020 in den USA auf breiter Basis kommerziell verfügbar sein wird.
Die CINtec PLUS-Zytologie liefert entscheidende Informationen darüber, welche HPV-positiven Frauen am meisten von einer sofortigen Überweisung zur Kolposkopie profitieren können. Dies ist ein wichtiger Schritt, um die Betreuung der Patientinnen zu individualisieren und sowohl eine Über- als auch eine Unterbehandlung zu verhindern.
„Eine beispielhafte Erfolgsgeschichte“ nennt Rainer Wessel, Chief Innovation Officer am DKFZ, die Entstehungsgeschichte des Testverfahrens. „Dank der Initiative der Firmengründer um Magnus von Knebel Doeberitz steht demnächst ein wichtiger Krebstest weltweit zur Verfügung, denn FDA-Zulassungen haben in der Regel Signalcharakter für die Zulassungsbehörden anderer Länder. Das Beispiel zeigt, dass Ausgründungen eine hervorragende Möglichkeit sind, vielversprechende Erfindungen aus der Grundlagenforschung zu einem marktfähigen Produkt weiterzuentwickeln. Das DKFZ unterstützt Erfinder auf diesem Weg in allen Phasen.“