Verklumpte, aggregierte und damit funktionsunfähige Proteinketten gelten als mitverantwortlich für zelluläre Alterungsprozesse und zahlreiche Krankheiten einschließlich neurodegenerativer Leiden wie zum Beispiel der Alzheimer-Demenz. Alle Organismen haben daher als „Chaperone“ bezeichnete Moleküle entwickelt, um solche schädlichen Aggregate wieder aufzulösen. Wie die Chaperone diese Aufgabe meistern, war allerdings weitgehend unbekannt.
Auf diese Frage haben Mario Avellaneda und Sander Tans am AMOLF-Institut in Amsterdam zusammen mit Bernd Bukau und Axel Mogk, Deutsches Krebsforschungszentrum und Universität Heidelberg, nun wichtige Antworten gefunden.
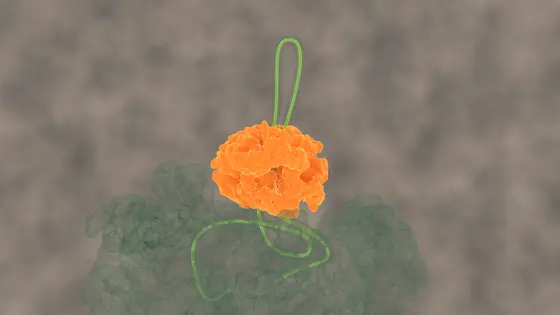
„Das ringförmige bakterielle Chaperon ClpB greift sich eine freie Schleife der Proteinkette, die aus dem Proteinaggregat herausragt, und zieht sie unter Aufwendung von Kraft durch seine zentrale Pore. Der gesamte Proteinklumpen ist zu groß, um durch die Pore zu passen. Durch die Zugkraft kann ClpB jedoch einzelne Proteinketten aus dem größeren Aggregat herausziehen. Das Chaperon funktioniert dabei wie eine Art Motor“, erläutert Bernd Bukau, dessen Arbeitsgruppe sowohl im Deutschen Krebsforschungszentrum als auch im Zentrum für Molekulare Biologie der Universität Heidelberg (ZMBH) angesiedelt ist.
Nach dem Herauslösen aus dem Aggregat kann sich die Proteinkette wieder zusammenfalten und normal funktionieren. Indem alle Proteine einzeln extrahiert werden, kann das Chaperon das gesamte Aggregat vollständig entwirren.
Die Forscher vermaßen die winzigen Bewegungen, die während der Proteinextraktion erfolgen, mit einer „optischen Pinzette“. Deren Funktion beruht darauf, dass Licht auf mikroskopische Objekte (z.B. Kügelchen) eine Kraft ausübt und diese dadurch bewegt werden können. Durch das Verankern einer Proteinkette zwischen zwei Kügelchen lassen sich so Strukturänderungen der Proteinkette messen. Dies ermöglichte den Forschern genau zu bestimmen, wie der ClpB-Motor Proteinketten transportiert. Wurden die mechanischen Hebel (aromatische Aminosäuren), die im Inneren der Pore von ClpB sitzen, durch Mutationen verändert, so verlor das Chaperon seine Zugkraft.
Die Wissenschaftler wollen als nächstes untersuchen, ob auch Chaperone aus menschlichen Zellen als Zugmaschinen für aggregierte Proteinketten wirken.
Mario J. Avellaneda, Kamila B. Franke, Vanda Sunderlikova, Bernd Bukau, Axel Mogk, Sander J. Tans: Processive extrusion of polypeptide loops by a Hsp100 disaggregase, Nature 2020, DOI: 10.1038/s41586-020-1964-y
Ein Video illustriert die Funktionsweise des Chaperons ClpB:
https://www.sandertanslab.nl/news/press-releases/avellaneda2020
Eine Illustration steht zum Download zur Verfügung:
still_image_cloop.png
BU: Das Chaperon ClpB zieht eine freie Proteinkette durch seine zentrale Pore
Nutzungshinweis für Bildmaterial zu Pressemitteilungen
Die Nutzung ist kostenlos. Das Deutsche Krebsforschungszentrum (DKFZ) gestattet die einmalige Verwendung in Zusammenhang mit der Berichterstattung über das Thema der Pressemitteilung bzw. über das DKFZ allgemein. Bitte geben Sie als Bildnachweis an: „Quelle: Avellaneda & Tans, AMOLF Amsterdam“.
Eine Weitergabe des Bildmaterials an Dritte ist nur nach vorheriger Rücksprache mit der DKFZ-Pressestelle (Tel. 06221 42 2854, E-Mail: presse@dkfz.de) gestattet. Eine Nutzung zu kommerziellen Zwecken ist untersagt.