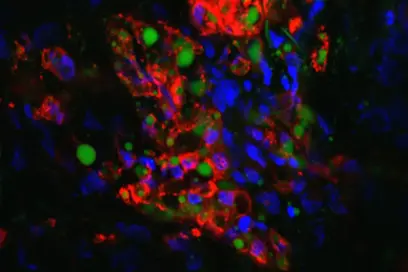
Blutgefäße spielen eine wichtige Rolle beim Wachstum und bei der Ausbreitung von Krebs. Die Zellen der Gefäßwand (Endothelzellen) und Krebszellen stehen in unmittelbarem Kontakt miteinander und beeinflussen sich gegenseitig. Diese Wechselwirkungen untersucht Andreas Fischer mit seinen Kollegen. Der Mediziner leitet eine Helmholtz-Hochschul-Nachwuchsgruppe, die sowohl im DKFZ als auch an der Medizinischen Fakultät Mannheim der Universität Heidelberg angesiedelt ist.
Fischer und sein Team hatten in Blutgefäßen von Tumoren überraschend große Mengen der aktivierten Form des Signalmoleküls Notch entdeckt. In Gefäßwandzellen aus Lungen-, Brust- oder Darmtumoren fanden sie deutlich mehr des aktivierten Rezeptors als in den entsprechenden gesunden Organen. Dabei stellten die Forscher fest: Je stärker Notch im Tumor-Endothel aktiviert war, desto weiter hatte sich der Krebs bereits ausgebreitet und desto schlechter war die Prognose für die Betroffenen.
Die Aktivierung des Rezeptorproteins Notch durch seine Bindungspartner ist ein wichtiger Kommunikationsweg, über den benachbarte Zellen Signale austauschen. Vom Fadenwurm über Insekten bis hin zum Menschen steuert Notch die Entstehung der Organe während der Embryonalentwicklung. Beim Erwachsenen reguliert das Signalprotein unter anderem die Aktivität der Blutstammzellen.
Dass fehlgesteuerte Notch-Signale Zellen entarten lassen können, etwa weiße Blutkörperchen zu Blutkrebs, konnten Krebsforscher schon vor einigen Jahren zeigen. Mit ihrer aktuellen Untersuchung haben Fischer und seine Kollegen jedoch erstmals nachgewiesen, dass auch die Notch-Aktivität von Zellen der unmittelbaren Umgebung des Tumors einen Einfluss auf die Krebserkrankung hat.
Fischer und Kollegen wiesen an Mäusen nach, dass es die Tumorzellen selbst sind, die im unmittelbaren Kontakt mit den Endothelzellen für die Notch-Aktivierung sorgen. Sie programmieren die Gefäßwandzellen für ihre eigenen Zwecke um und bereiten damit offenbar ihre Ausbreitung im Körper vor: Je stärker Notch im Tumor-Endothel aktiviert ist, desto mehr Krebszellen gelangen ins Blut und desto mehr Lungenmetastasen entstehen.
Überraschenderweise beschränkt sich die Notch-Aktivierung in tumortragenden Mäusen nicht auf die Blutgefäße im Tumor selbst, sondern betraf auch die Endothelzellen der Lunge. Offenbar schüttet der Tumor Signalstoffe aus, mit denen er die Ansiedelung seiner Metastasen vorbereitet.
Als Folge der Notch-Aktivierung steigern Endothelzellen die Produktion des Kontaktmoleküls VCAM1. Dieses Protein wirkt wie ein Druckknopf, der es den Krebszellen ermöglicht, sich an die Gefäßwand anzuheften und die Passage vorzubereiten. Zusätzlich erleichtert aktiviertes Notch den Krebszellen den Durchlass in die Blutbahn, indem es bestimmte dichtungsartige Strukturen zwischen den Gefäßwandzellen durchlässiger macht. Darüber hinaus bringt aktiviertes Notch die Endothelzellen dazu, Botenstoffe zu produzieren, die krebsfördernde Immunzellen in den Tumor locken.
„Zusammen ergeben die Ergebnisse ein eindeutiges Bild: Die Tumorzellen fördern auf vielfältige Weise ihre Ausbreitung im Körper, indem sie Notch aktiveren und damit die Endothelzellen zu ihren eigenen Zwecken umprogrammieren“, resümiert Andreas Fischer. „Daher wollten wir herausfinden, ob sich dieser verhängnisvolle Mechanismus unterbrechen lässt.“
Durch eine Blockade von Notch mit einem Antikörper, der aktuell in frühen klinischen Studien getestet wird, gelang es den Wissenschaftlern, in Mäusen die Ansiedlung von Krebszellen in der Lunge zu reduzieren. Auch die Blockade des Kontaktmoleküls VCAM1 mit einem Antikörper senkte die Anzahl von Lungenmetastasen und drosselte die Einwanderung krebsfördernder Immunzellen in den Tumor.
„Notch ist ein universelles Signalmolekül und lässt sich daher nur schlecht therapeutisch beeinflussen, ohne dabei lebenswichtige Prozesse zu stören“, sagt Andreas Fischer. „Aber ein gezielter kurzzeitiger Einsatz blockierender Antikörper könnte ein erfolgversprechender Ansatz sein, die gefährliche Ausbreitung von Tumoren zu unterdrücken. Das wollen wir mit unserer zukünftigen Arbeit weiterverfolgen.“
Elfriede Wieland, Juan Rodriguez-Vita, Sven S. Liebler, Carolin Mogler, Iris Moll, Stefanie E. Herberich, Elisa Espinet, Esther Herpel, Amitai Menuchin, Jenny Chang-Claude, Michael Hoffmeister, Christoffer Gebhardt, Hermann Brenner, Andreas Trumpp, Christian W. Siebel, Markus Hecker, Jochen Utikal, David Sprinzak, Andreas Fischer: Endothelial Notch1 activity facilitates metastasis. Cancer Cell 2017, DOI: 10.1016/j.ccell.2017.01.007