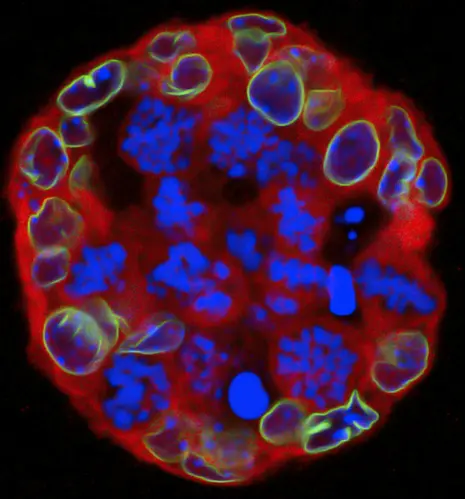
Bei den meisten Krebserkrankungen findet man in den Tumorzellen fehlerhafte Chromosomensätze. Zu dieser „Chromosomen-Instabilität “, wie Wissenschaftler das Phänomen bezeichnen, kommt es, wenn sich der vor der Zellteilung verdoppelte Chromosomensatz nicht gleichmäßig auf die beiden Tochterzellen verteilt. Chromosomen-Instabilität ist ein Indikator für einen ungünstigen Verlauf der Erkrankung und für schlechte Therapieerfolge.
Im scheinbaren Widerspruch zu dieser krebsfördernden Wirkung der falsch verteilten Chromosomen steht aber, dass Chromosomen-Instabilität eigentlich der Zelle schadet: Ihr Stoffwechsel gerät außer Kontrolle, weil Proteine in falschen Mengen produziert werden. In der Folge sterben die Zellen häufig durch den programmierten Zelltod Apoptose. Rocio Sotillo vom Deutschen Krebsforschungszentrum wollte nun am Beispiel Brustkrebs herausfinden, ob die Fehlverteilungen tatsächlich Krebs begünstigen oder hemmen.
Die Wissenschaftlerin und ihre Kollegen aktivierten in Brustdrüsenzellen der Maus das Krebsgen KRAS. Zahlreiche der so veränderten Tiere entwickeln im Laufe des Lebens Brustkrebs. Blockierten die Forscher bei diesen Mäusen das wachstumstreibende KRAS-Gen, so bildeten sich die Tumoren zurück.
Bei einer zweiten Gruppe von Mäusen aktivierten die Wissenschaftler zusätzlich zum wachstumstreibenden Krebsgen das Gen Mad2, das Chromosomen-Instabilität auslöst. Diese Tiere entwickelten später und seltener Tumoren in der Brust. Viele ihrer Brustdrüsenzellen unterbrachen die Zellteilung und starben durch Apoptose: Mit dieser Notmaßnahme versucht sich der Organismus vor den schädlichen Folgen ungleichmäßig verteilter Chromosomen zu schützen.
Jedoch schienen die anfängliche Auslese der Zellen letztendlich krebsfördernde Konsequenzen zu haben: Knapp ein Viertel der Tumoren in diesen Tieren wuchs weiter, auch nachdem die Forscher das wachstumstreibenden KRAS-Gens abgeschaltet hatten.
Rocio Sotillo und ihre Kollegen schlossen daraus, dass die Chromosomen-Fehlverteilung zu einer genetischen Vielfalt der Tumorzellen geführt hatte. Das begünstigt die Selektion einzelner Zellklone, die auch ohne den ursprünglichen Wachstumsstimulus des Krebsgens weiterwachsen können.
„Das hilft uns auch zu verstehen, warum Tumoren mit Chromosomen-Instabilität schlechter auf Therapien ansprechen: Die genetische Vielfalt der Tumorzellen steigert die Wahrscheinlichkeit, dass unter dem Selektionsdruck einer Krebsbehandlung therapieresistente Klone entstehen und sich durchsetzen können“, erklärt die Wissenschaftlerin.
Konstantina Rowald, Martina Mantovan, Joana Passos, Christopher Buccitelli, Balca R. Mardin, Jan O. Korbel, Martin Jechlinger, Rocio Sotillo: Negative selection and chromosome instability induced by Mad2 overexpression delay breast cancer but facilitate oncogene independent outgrowth.
CELL Reports 2016, DOI 10.1016/j.celrep.2016.05.048
Über das DKFZ
Das Deutsche Krebsforschungszentrum (DKFZ) ist mit mehr als 3.000 Mitarbeiterinnen und Mitarbeitern die größte biomedizinische Forschungseinrichtung in Deutschland. Wissenschaftlerinnen und Wissenschaftler erforschen im DKFZ, wie Krebs entsteht, erfassen Krebsrisikofaktoren und suchen nach neuen Strategien, die verhindern, dass Menschen an Krebs erkranken. Sie entwickeln neue Methoden, mit denen Tumoren präziser diagnostiziert und Krebspatienten erfolgreicher behandelt werden können. Beim Krebsinformationsdienst (KID) des DKFZ erhalten Betroffene, Interessierte und Fachkreise individuelle Antworten auf alle Fragen zum Thema Krebs.
Um vielversprechende Ansätze aus der Krebsforschung in die Klinik zu übertragen und so die Chancen von Patientinnen und Patienten zu verbessern, betreibt das DKFZ gemeinsam mit exzellenten Universitätskliniken und Forschungseinrichtungen in ganz Deutschland Translationszentren:
- Nationales Centrum für Tumorerkrankungen (NCT, 6 Standorte)
- Deutsches Konsortium für Translationale Krebsforschung (DKTK, 8 Standorte)
- Hopp-Kindertumorzentrum (KiTZ) Heidelberg
- Helmholtz-Institut für translationale Onkologie (HI-TRON) Mainz – ein Helmholtz-Institut des DKFZ
- DKFZ-Hector Krebsinstitut an der Universitätsmedizin Mannheim
- Nationales Krebspräventionszentrum (gemeinsam mit der Deutschen Krebshilfe)
Das DKFZ wird zu 90 Prozent vom Bundesministerium für Forschung, Technologie und Raumfahrt und zu 10 Prozent vom Land Baden-Württemberg finanziert und ist Mitglied in der Helmholtz-Gemeinschaft Deutscher Forschungszentren.