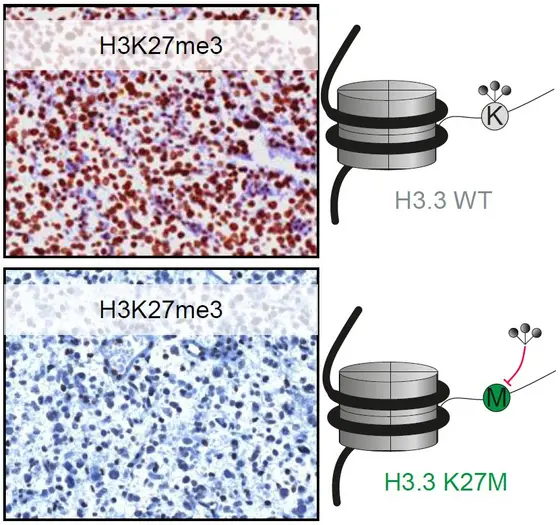
Zu den gefährlichsten Hirntumoren bei Kindern zählen die hochmalignen Gliome. Weniger als zehn Prozent der von dieser Erkrankung betroffenen Kinder und Jugendlichen überleben die ersten drei Jahre nach der Diagnose. Aus systematischen Analysen des Erbguts dieser Tumoren ist bekannt, dass circa die Hälfte der Fälle durch eine bestimmte Genveränderung gekennzeichnet ist: Die Mutation betrifft eines der Proteine zur DNA-Verpackung, das Histon H3.3. An Position 27 der Aminosäurekette wird die Aminosäure Lysin (K) durch ein Methionin (M) ersetzt („K27M-Mutation“).
Ein folgenreicher Austausch, der sich nicht nur auf das mutierte Verpackungsprotein selbst, sondern auch auf andere H3-Histonproteine auswirkt: In Tumorzellen führt die K27M-Mutation dazu, dass die Histonproteine deutlich weniger Methylgruppen tragen.
Im Deutschen Krebsforschungszentrum koordinierte Professor Stefan Pfister ein internationales Projekt, das erstmals die Folgen dieser K27M-Mutation bei bösartigen Gliomen untersuchte. Mit einem speziellen Immuntest prüften die Forscher zunächst den Methylierungsstatus der Histonproteine. So testeten sie Proben von über hundert aggressiven Gliomen, deren H3.3-Mutationsstatus bekannt war. Die Untersuchung zeigte, dass K27M-mutierte Gliome mit nahezu hundertprozentiger Wahrscheinlichkeit durch ihre geringe H3-Histonmethylierung identifiziert werden können.
In ihrer Arbeit beleuchteten die Forscher auch den Mechanismus, der die Histon-Methylierung beeinflusst: Das mutierte Histon H3.3 bindet ungewöhnlich stark an das Enzym EZH2, das für die Übertragung der Methylgruppen verantwortlich ist (Methyltransferase). Diese Bindung drosselt daraufhin die enzymatische Aktivität von EZH2.
Die K27M-Mutation wirkt sich nicht nur auf die Proteinmethylierung aus: Auch das Erbgut der mutierten Gliome ist weniger methyliert als das von Tumorzellen, die diese Mutation nicht tragen. Beide dieser epigenetischen Phänomene steigern wiederum die Genaktivität in diesen bösartigen Hirntumoren, was sich auf die Aggressivität der Tumoren auswirken kann.
„Auch bei anderen Krebsarten sind abweichende H3 Histon-Methylierungsmuster beschrieben, die in diesen Fällen häufig durch Defekte im Gen der Methyltransferase EZH2 selbst verursacht werden“, sagt Sebastian Bender, der Erstsautor der Arbeit. „In unserer Arbeit zeigen wir dagegen, wie sich eine spezifische genetische Veränderung in aggressiven Gliomen auf epigenetische Mechanismen wie Histon- und DNA-Methylierung auswirken kann.“
Sebastian Bender et al.: Reduced H3K27me3 and DNA Hypomethylation Are Major Drivers of Gene Expression in K27M-Mutant Pediatric High-Grade Gliomas. Cancer Cell 2013, DOI: 10.1016/j.ccr.2013.10.006