Bestimmte Variationen im Erbgut erhöhen das Risiko, an einem seltenen Knochenmarkkrebs, dem Multiplem Myelom, zu erkranken: Wissenschaftler aus Heidelberg und London haben das Erbgut von mehr als 4.600 Betroffenen nach charakteristischen Merkmalen durchsucht und dabei vier neue genetische Risikofaktoren entdeckt. Ein solcher Risikofaktor ist eine Variation in einem Abschnitt der Erbinformation (Gen), der beim Alterungsprozess von Zellen eine Rolle spielt. Die genetische Variante könnte gemeinsam mit anderen Faktoren bewirken, dass die Krebszellen sich der Alterung und dem vorgegebenen Zelltod entziehen, vermuten die Forscher. Die Ergebnisse wurden in der renommierten Fachzeitschrift „Nature Genetics“ veröffentlicht.
Die Studie ist ein gemeinsames Projekt von Arbeitsgruppen des Instituts für Krebsforschung am Royal Cancer Hospital in London, des Deutschen Krebsforschungszentrums (DKFZ) in Heidelberg (Abteilung Molekulargenetische Epidemiologie, Leiter: Professor Dr. Kari Hemminki) und der Sektion Multiples Myelom (Leiter: Professor Dr. Hartmut Goldschmidt) an der Medizinischen Universitätsklinik Heidelberg.
Molekulare Entstehung des Multiplen Myeloms noch wenig verstanden
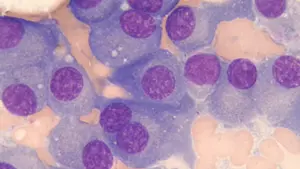
Das Multiple Myelom ist eine bösartige Erkrankung bestimmter Immunzellen, den sogenannten Plasmazellen, im Knochenmark. In Deutschland erkranken jährlich etwa 3.500 Menschen an der bisher meist unheilbaren Krebserkrankung des blutbildenden Systems. Die veränderten Plasmazellen vermehren sich im Knochenmark, stören die Blutbildung und schwächen die Knochensubstanz; Knochenbrüche, Blutarmut und Anfälligkeit für Infekte sind die Folgen. Die derzeit wirksamste Behandlung ist die Kombination von neuen Medikamenten mit einer Hochdosis-Chemotherapie, gefolgt von einer Transplantation mit patienteneigenen Blutstammzellen. In der Regel kehrt der Krebs jedoch nach einiger Zeit zurück.
„Die Erbgutanalyse gibt uns wichtige Hinweise auf die molekularen Prozesse innerhalb der Knochenmarkzellen, die bei der Entstehung des Multiplen Myeloms eine Rolle spielen“, erklärt Dr. Niels Weinhold von der Medizinischen Universitätsklinik Heidelberg, der in Zusammenarbeit mit Professor Hemminki vom DKFZ das Screening der deutschen Patientenproben koordinierte. „Wenn wir besser verstehen, wie Myelomzellen funktionieren und welche Eigenschaften sie haben, können wir in Zukunft neue Ansatzpunkte für Medikamente finden.“
Bestimmte Varianten im Erbgut treten bei Patienten häufiger auf als bei Gesunden
Wissenschaftler vermuten, dass die Erkrankung von verschiedenen Veränderungen im Erbgut hervorgerufen wird, die einzeln zwar unkritisch sind, ab einer bestimmten Anzahl und in Kombination aber die Fehlfunktion der Blutzellen verursachen. Um diese Variationen zu finden, verglich das internationale Forscherteam mit Hilfe eines speziellen Analyseverfahrens (genomweite Assoziationsstudie GWAS) das Erbgut (DNS) von 4.692 Patienten aus Deutschland und England mit Multiplem Myelom mit dem von 10.990 gesunden Menschen. Die Idee: Treten bestimmte genetische Variationen bei Patienten signifikant häufiger auf als bei der Kontrollgruppe, ist es wahrscheinlich, dass sie bei der Erkrankung eine Rolle spielen.
Die Wissenschaftler identifizierten in der aktuellen Studie vier solcher kritischen Variationen im Erbgut, vier entdeckten sie bereits in vorangegangen Analysen. In den DNS-Abschnitten, die diese Veränderung tragen, sind die genetischen Baupläne für eine ganze Reihe von Proteinen enthalten. Darunter befindet sich das Gen TERC, das die Länge der Schutzkappen am Ende größerer Erbguteinheiten, sogenannte Telomere, reguliert. Diese Schutzkappen werden bei jeder Zellteilung verkürzt. Sind sie abgetragen, büßt die Zelle bei der Teilung Stücke ihrer Erbinformation ein - sie altert und stirbt schließlich ab. Wird TERC außerplanmäßig aktiviert, wird dieser Prozess verlangsamt bzw. rückgängig gemacht. Die entdeckte Variation im Erbgut könnte diesen Regulationsmechanismus in den Tumorzellen beeinflussen. Welche Auswirkungen die genetischen Variationen genau haben, müssen weitere Untersuchungen klären.
Literatur:
Common variation at 3q26.2, 6p21.33, 17p11.2 and 22q13.1 influences multiple myeloma risk. Daniel Chubb, Niels Weinhold, Peter Broderick, Bowang Chen, David C Johnson, Asta Försti, Jayaram Vijayakrishnan, Gabriele Migliorini, Sara E Dobbins, Amy Holroyd, Dirk Hose, Brian A Walker, Faith E Davies, Walter A Gregory, Graham H Jackson, Julie A Irving, Guy Pratt, Chris Fegan, James A L Fenton, Kai Neben, Per Hoffmann, Markus M Nöthen, Thomas W Mühleisen, Lewin Eisele, Fiona M Ross, Christian Straka, Hermann Einsele, Christian Langer, Elisabeth Dörner, James M Allan, Anna Jauch, Gareth J Morgan, Kari Hemminki, Richard S Houlston & Hartmut Goldschmidt. Nat Genet. 2013 Aug 18. doi: 10.1038/ng.2733. [Epub ahead of print]