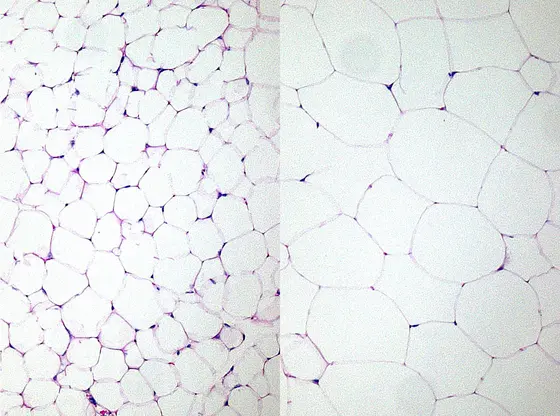
Weißes Fettgewebe ist die Energiereserve des Körpers. Hier wird überschüssiges Fett eingelagert, um in Hungerperioden andere Organe, besonders die Muskulatur, mit Energie zu versorgen. Nach Mahlzeiten sorgt Insulin dafür, dass Fettmoleküle aus dem Blut in die Speicher der Fettzellen eingelagert werden. Beim Fasten dagegen bewirken Adrenalin und Noradrenalin, dass das Fett zu Glycerol und Fettsäuren abgebaut wird. Ist dieses Gleichgewicht zwischen Speicherung und Abbau gestört, kann es zu Übergewicht, Adipositas und den damit verbundenen gesundheitsschädlichen Auswirkungen kommen: Das Fettgewebe produziert vermehrt Hormone, die das Übergewicht weiter fördern, die Entzündungsmarker steigen, und die Regulation des Blutzuckerspiegels gerät außer Kontrolle.
„Das sind die typischen Vorboten eines Typ2-Diabetes“, sagt Prof. Dr. Stephan Herzig. Der Stoffwechselexperte, der eine Brückenabteilung des Deutschen Krebsforschungszentrums, der Universität Heidelberg und des Universitätsklinikums Heidelberg leitet, sucht nach Schaltermolekülen, die zentrale Weichen des Stoffwechsels regulieren. Ein solcher Genschalter ist TBLR1. Wird er genetisch ausgeschaltet, so entwickeln Mäuse eine Fettleber, wie Herzig und sein Team kürzlich zeigten. Nun prüften die Heidelberger Forscher, ob TBLR1 in den Fettzellen die biochemischen Signalkaskaden startet, die letztlich in der Aktivierung der fettabbauenden Enzyme – der Lipasen – münden.
Die Forscher züchteten Mäuse, deren Fettzellen kein TBLR1 bilden können. Diese Tiere bauen auch nach 24-stündigem Fasten ihre Fettdepots nicht ab. Werden sie mit stark fetthaltiger Nahrung gefüttert, legen die TBLR1-negativen Mäuse viel mehr Gewicht zu als ihre gesunden Artgenossen. Gleichzeitig ist ihr Glukosestoffwechsel beeinträchtigt und das Fettgewebe enthält mehr Entzündungsmoleküle. „Insgesamt gerät der Fettstoffwechsel in einen kritischen, krankhaften Zustand“, fasst Stephan Herzig die molekularen Veränderungen zusammen.
Herzigs Team untersuchte daraufhin, ob TBLR1 auch beim Menschen den Fettabbau kontrolliert. Dazu analysierten die Forscher Fettgewebe von Frauen, die eine strikte Diät zur Gewichtsreduktion einhielten. Am Ende des Fastens enthielten deren Fettzellen viel mehr TBLR1-RNA als vor der Diät. Offensichtlich regt Hunger auch im menschlichen Organismus die Produktion des Genschalters an, der dann wiederum den Fettabbau ankurbelt. Gleichzeitig ging die Menge des Entzündungsmarkers CRP zurück und die Fettzellen produzierten mehr Hormone mit gesundheitsfördernder Wirkung.
„TBLR1 wirkt offensichtlich den schädlichen Stoffwechselveränderungen entgegen, die typisch für Übergewichtige sind und die zu schweren Erkrankungen führen können“, so Stephan Herzig. Langfristiges Ziel seiner Forschung ist, über Schaltermoleküle wie etwa TBLR1 einen aus der Balance geratenen Energiestoffwechsel gezielt zu beeinflussen.
Maria Rohm, Anke Sommerfeld, Daniela Strzoda, Allan Jones, Tjeerd Sijmonsma, Gottfried Rudofsky, Christian Wolfrum, Carsten Sticht, Norbert Gretz, Maximilian Zeyda, Lukas Leitner, Peter Nawroth, Thomas Stulnig, Mauricio Berriel Diaz, Alexandros Vegiopoulos und Stephan Herzig: Transcriptional co-factor TBLR1 controls lipid mobilization in white adipose tissue. Cell Metabolism 2013, doi: 10.1016/j.cmet.2013.02.010.
Ein Bild zur Pressemitteilung steht im Internet zur Verfügung unter:
WAT-lean-obese.jpg
BU: Weißes Fettgewebe von schlanken (links) und adipösen Mäusen
Quelle: Maria Rohm, Deutsches Krebsforschungszentrum