Proteine sind wichtige Werkzeuge unseres Körpers: Sie verleihen ihm Struktur, beschleunigen chemische Reaktionen, transportieren wichtige Stoffe, schützen vor Krankheitserregern oder dienen im Notfall als Energielieferant. Wenn sich aber die Menge eines Proteins stark erhöht oder reduziert, sind häufig Krankheiten die Folge. Wird beispielsweise das Proteins p53, auch „Wächter des Genoms“ genannt, unkontrolliert abgebaut, kann in der betroffenen Zelle weder ein Schaden an der DNA repariert, noch die Zellteilung reguliert oder der Zelltod eingeleitet werden. Dadurch beginnt sich die fehlerhafte Zelle unkontrolliert zu teilen, ein Tumor entsteht. Um beurteilen zu können, ob der Proteinstoffwechsel einer Zelle gestört ist, haben Forscher um Prof. Michael Knop eine neue Methode entwickelt: Sie bringen die Proteine zum Leuchten. Aber nicht – wie bisher üblich – mithilfe nur eines Fluoreszenzfarbstoffs, sondern mit einem Komplex aus einem rot und einem grün fluoreszierenden Marker. Dieser sogenannte Tandem-Fluoreszenzprotein-Timer (tFT) wird schon während der Proteinentstehung an das Protein gekoppelt und gibt den Forschern so Aufschluss über Menge, Aufenthaltsort und Alter der Moleküle.
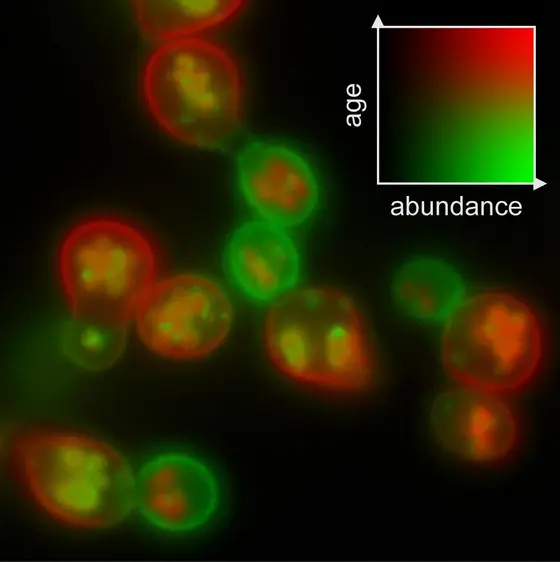
Michael Knop, Leiter der Arbeitsgruppe Zellmorphogenese und Signalübermittlung in der DKFZ-ZMBH-Allianz, erklärt, wie das neue Verfahren funktioniert: „Unmittelbar nachdem die Zelle das Protein gebildet hat, beginnt der grüne Farbstoff – bestehend aus dem grün fluoreszierenden Protein GFP – zu leuchten. Überall dort, wo es in der Zelle grün leuchtet, ist das Molekül also zu finden. Anhand der Farbintensität ist es zudem möglich, die Proteinmenge zu bestimmen.“ Aber auch auf das Alter der Moleküle können die Wissenschaftler nun schließen. „Mit fortschreitender Zeit fängt auch das rot fluoreszierende Protein zu leuchten an. Dadurch verfärben sich die Proteine von grün nach rot, je älter sie werden“, erläutert Knop weiter. „Damit sind neu gebildete – grüne – von alten – roten – Proteinen unterscheidbar. So können wir deren Lebensdauer berechnen und überprüfen, ob ein Protein schneller oder langsamer als gewöhnlich abgebaut wird.“ Ein weiterer Pluspunkt: Die tFTs fluoreszieren sehr hell, dadurch ist der Nachweis sehr empfindlich.
Mithilfe der neuen tFTs ist es möglich, das Alter von Proteinen in einem Zeitrahmen von zehn Minuten bis zu mehreren Stunden zu bestimmen. Wird der grüne Farbstoff GFP mit verschiedenen Fluoreszenzfarbstoffen kombiniert, können sogar über mehrere Tage andauernde Abbauprozesse verfolgt werden. Als Modellorganismus wählten die Wissenschaftler die Hefe. Der Grund: Der Einzeller ist unseren Zellen in vielen grundlegenden Prozessen sehr ähnlich und daher als Model gut geeignet. Prof. Elmar Schiebel, Leiter der Arbeitsgruppe Chromosomen Segregation in der Zellteilung in der DKFZ-ZMBH-Allianz, hat mit seinen Mitarbeitern zudem gezeigt, dass dieses Verfahren auch in menschlichen Zellen funktioniert. Dadurch eröffnen sich ganz neue Perspektiven für die Untersuchung geschädigter Zellen und für die Entwicklung neuer Medikamente, um die Proteinstabilität in kranken Zellen zu regulieren.
Anton Khmelinskii, Philipp J Keller, Anna Bartosik, Matthias Meurer, Joseph D Barry, Balca R Mardin, Andreas Kaufmann, Susanne Trautmann, Malte Wachsmuth, Gislene Pereira, Wolfgang Huber, Elmar Schiebel & Michael Knop: Tandem fluorescent protein timers for in vivo analysis of protein dynamics. Nature Biotechnology, 2012, DOI: 10.1038/nbt.2281
Ein Bild zur Pressemitteilung steht im Internet zur Verfügung unter:
farbstoff-timer.jpg
Bildunterschrift: Der neue Timer-Farbstoff macht sichtbar, dass die Mutterzelle die älteren Proteine (rot) behält, die Tochterzelle dagegen neue Moleküle (grün) bildet.