Sobald sie die Größe eines Stecknadelkopfes erreicht haben, sind Tumoren auf neue Blutgefäße angewiesen. Diese Neubildung von Adern bezeichnen Wissenschaftler als Angiogenese. In diesen Prozess einzugreifen („Anti-Angiogenese“) gilt als vielversprechender Ansatz in der Krebsmedizin. Die bereits verfügbaren Medikamente, die verhindern, dass neue Blutkapillaren aussprossen, blieben allerdings hinter den hochgesteckten Erwartungen zurück.
Eine bessere Wirksamkeit erhoffen Mediziner von anti-angiogenen Therapien, die die Gefäßentstehung von mehreren Seiten gleichzeitig angreifen. Die heute verfügbaren Medikamente richten sich gegen VEGF, den Gefäßwachstumsfaktor, der neue Blutbahnen sprossen lässt. Eine wichtige Rolle in der Angiogenese spielen jedoch auch die beiden Signalmoleküle Angiopoietin-1 und Angiopoietin-2. Ang-1 sorgt dafür, dass die Gefäße ausreifen, während Ang-2 als funktioneller Gegenspieler von Ang-1 wirkt. Beide Signalmoleküle binden an den gleichen Rezeptor, Tie-2, auf der Oberfläche von Gefäßwandzellen.
„Es gibt bereits Arbeiten, die zeigen, dass Ang-2 ein geeignetes Zielmolekül für neue Therapien ist, die sich gegen die Blutversorgung von Tumoren richten. Als aussichtsreich gelten vor allem Kombinationen mit den bereits zugelassenen anti-angiogenen Medikamenten“, sagt Prof. Dr. Hellmut Augustin, dessen Arbeitsgruppen sowohl im Deutschen Krebsforschungszentrum als auch an der Medizinischen Fakultät Mannheim der Universität Heidelberg angesiedelt sind. „Aber weil die Rolle von Ang-2 noch nicht ganz klar war, mussten wir zunächst den molekularen Wirkmechanismus besser verstehen.“
Die Wissenschaftler in Augustins Arbeitsgruppe fanden nun heraus, dass Gefäßwandzellen an der Spitze sprossender Kapillaren sehr viel Ang-2 produzieren, nicht aber dessen bekannten Rezeptor Tie-2. Trotzdem reagieren diese Zellen auf das Signalmolekül. Möglicherweise, so schlossen Forscher daraus, kann Ang-2 auch über andere Oberflächenmoleküle als Tie-2 Signale an die Gefäßwandzellen übermitteln.
Und tatsächlich erkannten die Gefäßexperten bei den Zellen an der Spitze der neu entstehenden Kapillaren, dass Ang-2 die so genannten Integrine als alternativen Rezeptor nutzen kann. Integrine sind auf vielen Zelltypen verbreitete Membranproteine, die an zahlreichen Signalübertragungen zwischen Zellen beteiligt sind.
„Wir haben es also mit zwei voneinander unabhängigen Wirkungen zu tun“, erklärt Hellmut Augustin: „einerseits die bereits bekannte Funktion als Gegenspieler von Ang-1 in Gefäßwandzellen, die den Rezeptor Tie-2 produzieren, andererseits die Integrin-abhängige Wirkung auf die Zellen der Kapillarspitze, die kein Tie-2 haben. Das erklärt uns auch, warum experimentelle Therapien gegen Ang-2 erfolgreicher sind als gegen seinen bisher bekannten Rezeptor Tie-2. Dieses Ergebnis zeigt uns, dass es sich doppelt lohnt, Therapien gegen Ang-2 weiterzuentwickeln: Damit könnten wir die Bildung von Blutgefäßen im Tumor von zwei Seiten zugleich angreifen.“
Moritz Felcht, Robert Luck, Alexander Schering, Philipp Seidel, Kshitij Srivastava, Junhao Hu, Arne Bartol, Yvonne Kienast, Christiane Vettel, Elias K. Loos, Simone Kutschera, Susanne Bartels, Sila Appak, Eva Besemfelder, Dorothee Terhardt, Emmanouil Chavakis, Thomas Wieland, Christian Klein, Markus Thomas, Akiyoshi Uemura, Sergij Goerdt und Hellmut G. Augustin: Angiopoietin-2 differentially regulates angiogenesis through TIE2 and integrin signaling. Journal of Clinical Investigations 2012, DOI: 10.1172/JCI58832
Ein Bild zur Pressemitteilung steht im Internet zur Verfügung unter:
Networkstructure.jpg
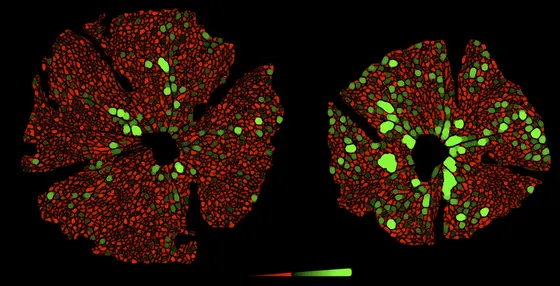
Quelle: Hellmut Augustin, Deutsches Krebsforschungszentrum
Legende: Nach der Geburt wachsen bei der Maus die Blutgefäße zentrifugal in die Netzhaut ein. Nach Blockade von Angiopoietin-2 (rechts) weist das Gefäßnetz der Netzhaut mehr Lücken (grün, >40µm) auf und die Retina wächst langsamer.