Forschende des Deutschen Krebsforschungszentrums (DKFZ) und der Klinik für Anästhesiologie des Universitätsklinikums Heidelberg (UKHD) berichten in ihrer aktuellen Publikation von einem neuen Ansatz, eine Sepsis mit hoher Genauigkeit zu erkennen. Sepsis ist die dritthäufigste Todesursache in Deutschland und eine der schwerwiegendsten Komplikationen bei onkologischen OPs. „Unsere Ergebnisse zeigen, dass sich mithilfe der hyperspektralen Bildgebung und KI-gestützter Analysen eine Sepsis schnell und sogar ohne Blutabnahme diagnostizieren lässt“, erklärt Lena Maier-Hein, Abteilungsleiterin am DKFZ und Direktorin am NCT Heidelberg, die die Studie gemeinsam mit zwei Kollegen vom UKHD leitete.
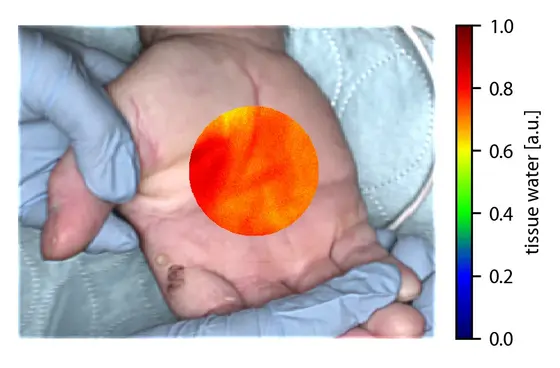
Unter hyperspektraler Bildgebung verstehen Experten eine Kameratechnik, die verschiedene Bereiche des elektromagnetischen Spektrums auch jenseits der sichtbaren Wellenlängen abbildet und dadurch Unsichtbares sichtbar machen kann.
Haut als Spiegel der Mikrozirkulation
„Ein kritischer Aspekt der Sepsisbehandlung ist die frühzeitige und genaue Diagnose, bevor anhaltende Organfunktionsstörungen auftreten“, erklärt Markus A. Weigand, Direktor der Klinik für Anästhesiologie des UKHD und Generalsekretär der Deutschen Sepsis Gesellschaft, der die Studie gemeinsam mit Lena Maier-Hein und seinem Kollegen Maximilian Dietrich leitete. Diese Herausforderung wird durch die unspezifischen Anzeichen und Symptome des Sepsis-Syndroms erschwert, da zuverlässige Biomarker, die eine Sepsis eindeutig anzeigen, bislang fehlen.
„Die Durchblutung kleinster Blutgefäße – die sogenannte Mikrozirkulation – verändert sich bereits in einem sehr frühen Stadium einer Sepsis. Gleichzeitig führt die Entzündungsreaktion im Körper dazu, dass die Wände der Blutgefäße durchlässiger werden, sodass Flüssigkeit ins umliegende Gewebe austritt. Diese Prozesse lassen sich mit der entwickelten Technologie innerhalb weniger Sekunden sichtbar machen. Da sie ähnlich wie eine Fotoaufnahme funktioniert, bedeutet sie keine Belastung für die Patientinnen und Patienten“, so Maximilian Dietrich, Intensivmediziner der Klinik für Anästhesiologie des UKHD.
Die Forschenden setzten in der Studie ein speziell entwickeltes KI-basiertes Kamerasystem ein, das die Lichtreflexion der Haut an Handflächen und Fingern erfasst. Das reflektierte Licht lässt sich zur Beurteilung der Mikrozirkulation nutzen, da es sensitiv auf Änderungen in der Konzentration von Wasser, Blut und Sauerstoff reagiert. So lassen sich die hochdimensionalen – nicht von Menschen interpretierbaren – Messdaten mittels neuronaler Netze in klinisch relevante Information überführen.
Besser als etablierte Scores und Biomarker
In einer prospektiven Studie auf der interdisziplinären operativen Intensivstation des Universitätsklinikums Heidelberg wurden bei über 480 kritisch kranken Patientinnen und Patienten hyperspektrale Bilder der Handflächen und Finger aufgenommen. Eine darauf trainierte KI konnte Sepsis anhand dieser Daten mit hoher Genauigkeit identifizieren: Die Vorhersagegüte* lag bei 0,80. Wurden zusätzlich einfach verfügbare klinische Daten wie Vitalparameter in die Analyse einbezogen, stieg der Wert auf 0,94. Auch die Vorhersage der 30-Tage-Sterblichkeit gelang mit hoher Genauigkeit.
„Im Vergleich zu klassischen klinischen Bewertungsinstrumenten, die auf Parametern wie mentalem Status, Atmungsfrequenz und Blutdruck beruhen (z. B. qSOFA), oder auf Entzündungs-Biomarkern wie C-reaktivem Protein und Procalcitonin, bietet das neue Verfahren Vorteile. Besonders in zeitkritischen Situationen oder bei hohem Patientenaufkommen können KI-gestützte Tools ein schnelles und zuverlässiges Sepsis-Screening ermöglichen“, erklärt Silvia Seidlitz, Wissenschaftlerin am DKFZ und Erstautorin der Veröffentlichung.