Bei der Entfernung eines Tumors entscheiden oft wenige Millimeter über den Erfolg der Operation: Schneidet die Chirurgin oder der Chirurg zu nah am Tumor, können Krebszellen im Körper verbleiben. Wird ein größerer Abstand gewählt, können wichtige umliegende Strukturen wie Nerven geschädigt werden. Zur stichprobenartigen Beurteilung des Tumorrands dienen bislang vor allem Gewebeproben, die während einer Operation entnommen und unmittelbar feingeweblich durch die Pathologie auf verbliebene Tumorzellen untersucht werden. Künftig soll eine Weiterentwicklung der Fluoreszenzbildgebung neue Maßstäbe für die hochpräzise Tumorchirurgie setzen.
„Könnten Chirurgen bereits während der Operation sicher zwischen Tumorgewebe und gesunden Strukturen unterscheiden, so ließen sich die Heilungschancen für die Betroffenen in vielen Fällen deutlich verbessern. Das DKFZ hat sich daher intensiv dafür eingesetzt, am NCT-Standort Dresden eine Professur für funktionelle Bildgebung einzurichten. Wir gehen davon aus, dass die Weiterentwicklung dieser bildgebenden Verfahren in Zukunft vielen Patientinnen und Patienten direkt zugute kommen kann“, sagt Prof. Michael Baumann, der Vorstandsvorsitzende des DKFZ.
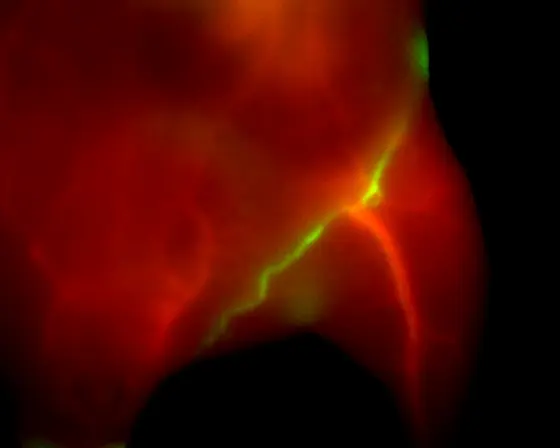
Bei der Fluoreszenzbildgebung bringt infrarotes Licht in Kombination mit speziellen Farbstoffen Gewebe, Gefäße oder Körperflüssigkeiten zum Leuchten. Bislang funktioniert die nicht-invasive Methode mit Infrarotlicht mit Wellenlängen von 700 bis 900 Nanometern und wird beispielsweise genutzt, um während einer Operation den Blutfluss in neu verbundenen anatomischen Strukturen zu überprüfen. Bruns und sein Team setzen hingegen auf kurzwelliges Infrarotlicht (auch SWIR von englisch short-wave-infrared) mit Wellenlängen größer 1.000 Nanometern. „Kurzwelliges Infrarotlicht bietet einen besseren Kontrast und schärfere Bilder. Ausgehend von unseren Erkenntnissen aus der Grundlagenforschung sind wir davon überzeugt, dass die Methode das Potential hat, in Zukunft verbliebene Krebszellen an Tumorrändern in einer Tiefe von mehreren Millimetern abzubilden. Auch das Sichtbarmachen einiger weniger Tumorzellen in Lymphknoten liegt im Bereich des Möglichen“, sagt Prof. Oliver Bruns (42), der seit dem 1. Februar die neu geschaffene Professur für Funktionelle Bildgebung in der Operativen Onkologie am Nationalen Centrum für Tumorerkrankungen Dresden (NCT/UCC) bekleidet.
„Die Darstellung einzelner Tumorzellen im gesamten Tumorrand und in Lymphknoten während einer Operation ist bislang ein ungelöstes Problem. Die Idealvorstellung wäre, dass die neue Bildgebungsmethode künftig so präzise ist, dass beispielsweise Tumorzellen rot erscheinen, Nerven grün und Blutgefäße blau. Wenn die Entwicklung in diese Richtung geht, könnte sich die Präzision und Sicherheit in der Tumorchirurgie deutlich erhöhen“, betont Prof. Jürgen Weitz, Mitglied im geschäftsführenden Direktorium des NCT/UCC und Direktor der Klinik für Viszeral-, Thorax- und Gefäßchirurgie des Universitätsklinikums Carl Gustav Carus Dresden.
Ein Grund dafür, dass sich die SWIR-Bildgebung für die Medizin erst in jüngster Zeit zu einem schnell wachsenden Forschungsgebiet entwickelt hat, liegt darin, dass es bis vor Kurzem keine hierfür geeignete bildgebende Technik gab. Die rasante Kameraentwicklung in der Industrie – etwa im Bereich des autonomen Fahrens – hat nun aber die nötigen technischen Grundlagen geschaffen und für die klinische Forschung und Anwendung erschwinglich gemacht. Des Weiteren gibt es bislang nur wenige für die klinische Anwendung zugelassene – auch für die SWIR-Bildgebung geeignete – Fluoreszenzfarbstoffe, mit denen sich bestimmte Gewebe und Strukturen, wie Tumoren oder Blutgefäße, gezielt sichtbar machen lassen. „Meine Vision ist, dass in zehn bis zwanzig Jahren jede große Klinik die SWIR-Bildgebung einsetzt und über die nötigen technischen Voraussetzungen und geeigneten Kontrastmittel verfügt“, sagt Prof. Bruns, der zuletzt eine Forschungsgruppe am Helmholtz Pioneer Campus in München leitete.
Um dieses Ziel zu erreichen, will der Wissenschaftler am Dresdner Uniklinikum zunächst die aktuell verfügbaren klinischen Möglichkeiten der Fluoreszenzbildgebung für verschiedene onkologische Operationen erweitern. Hierauf aufbauend sollen dann Schritt für Schritt die technologischen Voraussetzungen geschaffen werden, um mit kurzwelligem Infrarotlicht zu arbeiten. „Uns ist es sehr wichtig, das unmittelbare Feedback der Chirurginnen und Chirurgen zu erhalten. Etwa dazu, bei welchen Fragestellungen die neue Methode besonders benötigt wird und wie gut die Anwendung funktioniert. Die Möglichkeit, unsere Forschung auf direktem Weg in die Klinik zu überführen und die Aufbruchsstimmung unter den chirurgischen Kolleginnen und Kollegen, die hier gemeinsam mit uns neue Wege gehen wollen, waren ein wesentlicher Grund für mich, nach Dresden zu kommen“, sagt Bruns. „Mit Oliver Bruns konnten wir einen ausgewiesenen Bildgebungsexperten für den Hochschulmedizinstandort Dresden gewinnen“, so Prof. Michael Albrecht, Medizinischer Vorstand des Universitätsklinikums Dresden. „Wir sind überzeugt, durch seine wissenschaftliche Expertise die Präzision der Krebschirurgie weiter vorantreiben zu können.“ Auch über die Krebschirurgie hinaus bietet die Technik Anwendungsmöglichkeiten und könnte künftig beispielsweise auch bei bestimmten Screening-Untersuchungen wie Darmspiegelungen zum Einsatz kommen.
Bruns, der seit Jahren als Pionier auf dem Gebiet der SWIR-Bildgebung forscht, arbeitet bei der Entwicklung neuer Farbstoffe und der Integration neuester technologischer Entwicklungen in medizinische Bildgebungseinheiten eng mit Forschergruppen auf der ganzen Welt zusammen, etwa von der Stanford University, der University of California (Los Angeles), dem National Cancer Institute (NCI/NIH, Maryland), dem Imperial College London und der Universität Hannover. „Wir sind überzeugt davon, dass die neue Technologie deutlich besser ist als der derzeitige Standard. Deshalb ist es wichtig, alle Kräfte – auch gemeinsam mit verschiedenen Dresdner Forschungsinstitutionen – zu bündeln, um möglichst bald zu verbesserten Therapien zu gelangen“, so Bruns.
Oliver Bruns, Jahrgang 1980, studierte Biochemie und Molekularbiologie an der Universität Hamburg und promovierte am Universitätsklinikum Hamburg-Eppendorf. Er forschte als wissenschaftlicher Mitarbeiter am Leibniz-Institut für Experimentelle Virologie in Hamburg und über mehrere Jahre am Massachusetts Institute of Technology (MIT). 2018 wurde er Principal Investigator am Helmholtz Pioneer Campus in München und wird im Rahmen des Emmy Noether-Programmes von der Deutschen Forschungsgemeinschaft (DFG) gefördert. Oliver Bruns erhielt bereits eine Reihe wissenschaftlicher Auszeichnungen und Förderungen, darunter die Emmy Noether-Nachwuchsgruppenleitung, ein Long-Term Fellowship der European Molecular Biology Organisation (EMBO) sowie die Karl-Heinz Hölzer-Auszeichnung für interdisziplinäre Forschung (2010). Er koordiniert ein von der Chan-Zuckerberg-Initiative (CZI) mit einer Millionen Dollar gefördertes Konsortium und wird seit diesem Jahr vom Bundesministerium für Bildung und Forschung (BMBF) im Rahmen des BetterView Verbundes (Projektvolumen: 4,1 Mio. Euro) gefördert. Oliver Bruns ist Autor von 43 Publikationen und hält 13 Patente.