Stammzellen und Krebs
- Zell- und Tumorbiologie

Prof. Dr. Andreas Trumpp
Abteilungsleiter "Stammzellen und Krebs", Geschäftsführer des Stammzellinstituts "HI-STEM gGmbH"
Unsere Arbeit zielt auf Krebsstammzellen (CSCs) ab - mutierte Stammzellen, die Tumorwachstum, Wiederauftreten und Therapieresistenz vorantreiben. Wir untersuchen, wie diese malignen Zellen Plastizität nutzen, um sich anzupassen und Behandlungen zu entgehen, und decken dabei Zusammenhänge zwischen Stammzellprogrammen, Plastizität und neuronaler Einwirkung auf. Wir entwickeln dadurch personalisierte Präzisionstherapien der nächsten Generation, um den Krebs durch CSCs zu stoppen.
Bild: © Ömer Copur
Bild: © Ömer Copur
Unsere Forschung
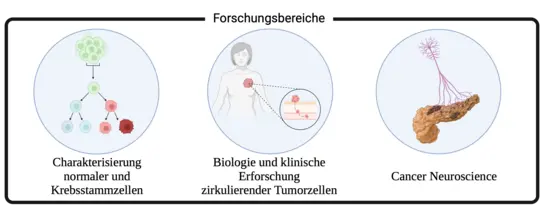
Unsere Gruppe untersucht die Biologie normaler und maligner Stammzellen. Während Stammzellen durch Selbsterneuerung und Differenzierung Gewebe erhalten und regenerieren, verwandeln Mutationen und deregulierte Netzwerke sie in Krebsstammzellen (CSCs). Ihre Plastizität und klonale Regenerationsfähigkeit stellen große Herausforderungen für die Onkologie dar, darunter Förderung von Tumorwachstum und Metastasen, sowie Entwicklung von gefürchteter Therapieresistenz und Rezidivierung.
Unser Ziel ist es, die molekularen Schwachstellen von CSCs und die durch Stammzellen vermittelte Plastizität aufzudecken und diese Erkenntnisse in neue innovative therapeutische Diagnose- und Behandlungsstrategien zu entwickeln. Unsere Forschung umfasst vier miteinander verbundene Hauptbereiche:
- Hämatopoetische Stammzellen – Mechanismus der Selbsterneuerung, Multipotenz und Differenzierung
- Leukämische Stammzellen bei AML – Mechanismen der Resistenz und der Rezidivbildung
- Zirkulierende Tumorzellen und Metastasen- initiierende Stammzellen bei Brustkrebs –Verbesserung der Präzisions-Onkologie
- „Cancer Neuroscience“ – Wie periphere Nerven das Fortschreiten und die Metastasierung von Bauchspeicheldrüsenkrebs und anderen Karzinomen beeinflussen
Wir kombinieren modernste Methoden – darunter Einzelzell-Multi-Omics- und Metabolomische-Technologien, Multi-parameter Durchfluss-Zytometrie, Fortgeschrittene Mikroskopietechniken, CRISPR-Gen-Editing, gentechnisch veränderte Mausmodelle, aus Patienten gewonnene Organoide und PDX-Modelle aus longitudinal gewonnenen klinischen Proben –, um grundlegende Erkenntnisse mit präklinischer und klinischer Umsetzung zu verbinden. Unsere Vision ist es, diese Entdeckungen in neuartige Echtzeit-Diagnostik und innovative Therapien umzusetzen, die die Überlebensrate und Lebensqualität von Krebspatienten verbessern.

Wichtige Forschungsergebnisse & Auswirkungen
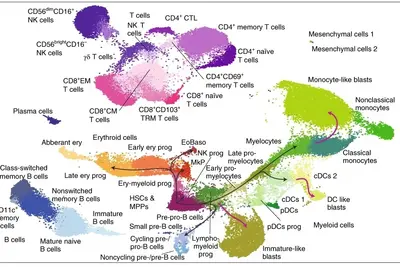
Hämatopoetische Stammzellen (HSC) sorgen aufgrund ihrer Fähigkeit zur umfassenden Selbsterneuerung und Multipotenz für die lebenslange Produktion aller Blutzellen. Darüber hinaus sind HSCs entscheidend für die Regeneration des Blutsystems, wie z.B. nach Stresszuständen wie Entzündungen, Blutverlust oder toxischen Belastungen wie Chemotherapie, verantwortlich.
→ Bedeutende Entdeckung des Trumpp-Teams: Charakterisierung „schlafender“ (dormanter) HSCs als stressresistente Stammzellreserve und Entwicklung des international anerkannten „Waddington“-Modells einer kontinuierlichen Hämatopoese mit HSCs an der Spitze der Hierarchie, aus denen lineage-primed Vorläufer und reife Blutzellen hervorgehen.
Entdeckung und erste Charakterisierung schlafender, dormanter HSCs: Die Ruhephase schützt ihre genomische Integrität und vermittelt die Resistenz gegenüber Chemotherapie. Entzündungssignale (z.B. Interferone, Interleukine) oder Blutverlust aktivieren schlafende HSCs und diese leiten die Regeneration der verlorenen Blutzellen ein (Wilson et al., Cell 2008, Essers et al., Nature 2009, Walter et al., Nature 2015).
Identifizierung von Regulatoren die die Funktion und Plastizität von schlafenden HSCs-regulieren: MYC, Retinsäure, Netrin-1 und alternative mRNA Polyadenylierung (Wilson et al., Genes & Development 2004, Scognamiglio et al., Cell 2016, Cabezas-Wallscheid et al., Cell 2017, Bahr et al., Nature 2018, Sommerkamp et al., Cell Stem Cell 2020).
Zusammen mit dem Team von Lars Steinmetz (EMBL) und Marieke Essers (HI-STEM) haben wir ein, inzwischen international anerkanntes, kontinuierliches Hämatopoese-Modell (Waddington) entwickelt, das das klassische „Tree-model“ für die Blutbildung abgelöst hat (Velten et al., Nature Cell Biology 2017).
Wir entdeckten, dass HSCs als Antigen-präsentierende Zellen fungieren können und es daher einen immunologischen Kontrollmechanismus durch CD4 T Zellen gibt, der veränderte HSCs erkennt und frühzeitig eliminiert (Hernàndez-Malmierca et al., Cell Stem Cell 2022).
Unser Team etablierte die MPP1-6-Nomenklatur für Blut-Vorläuferzellen unmittelbar nach den HSCs und charakterisierte deren Funktionen (Cabezas-Wallscheid et al., Cell Stem Cell 2014, Sommerkamp et al., Blood 2021).
Das Trumpp Team identifizierte eine neue, hochgradig ruhende HSC mit lymphoiden Eigenschaften, die im Alterungsprozess eine wichtige Rolle spielt (Lin et al., in Überarbeitung 2026).

Die akute myeloische Leukämie (AML) ist eine aggressive hämatologische Neoplasie, bei der Krankheitsentstehung, Therapieresistenz und Rezidivbildung maßgeblich durch leukämische Stammzellen (LSCs) getrieben werden. Das LSC-Kompartiment ist hochgradig heterogen, was wesentlich zur variablen Therapieantwort beiträgt. Diese Heterogenität beruht auf genetischen und nicht-genetischen Faktoren, darunter somatische Mutationen, die Zelle des Ursprungs, transkriptionelle und epigenetische Zustände sowie ausgeprägte phänotypische Plastizität. Therapieresistente LSCs überleben die Behandlung, treiben klonale Evolution voran und sind verantwortlich für Krankheitsprogression und Rezidive.
Neben intensiven und häufig hochtoxischen Standard-Kombinationschemotherapien verändert die Therapie mit dem BCL-2-Inhibitor Venetoclax in Kombination mit hypomethylierenden Substanzen (z. B. 5-Azacytidin) derzeit grundlegend die AML-Behandlung und wird voraussichtlich auch als Erstlinientherapie etabliert werden. Wir haben kürzlich den MAC-Score entwickelt, ein personalisiertes prädiktives Biomarkersystem, das eine Vorhersage des Ansprechens bzw. der Resistenz von AML-Patientinnen gegenüber Venetoclax-basierten Therapien ermöglicht.
→ Bedeutende Entdeckung des Trumpp-Teams: Charakterisierung der genetischen und nicht-genetischen Heterogenität von AML-Stammzellen bei Patienten auf molekularer und zellulärer Ebene. Entwicklung von MAC-Scoring, dem ersten klinisch nutzbaren Biomarker zur hochpräzisen Vorhersage des Ansprechens von Patienten auf Venetoclax.
Identifizierung von BCAT1 als metabolischer Treiber von LSCs: Das BCAT1 Enzym steuert den Katabolismus verzweigtkettiger Aminosäuren. BCAT-1 Überexpression in LSCs hat eine ähnliche Funktion wie IDH/TET2-Mutationen und ist ein Resistenzmechanismus bei AML Patienten unter IDH-Inhibitor Therapie (Raffel et al., Nature 2017, Raffel et al., Blood 2020).
Zusammen mit dem Team von Claudia Lengerke und Helmut Salih (Universitätsklinikum Tübingen) konnten wir die Resistenz von LSCs gegenüber Natürlichen-Killerzellen aufdecken und zeigen, dass eine PARP1-Hemmung die NK-Kontrolle wiederherstellt (Paczulla et al., Nature 2019) – eine klinischen Studie, NAKIP-AML, ist in Planung.
Durch Einzelzell-Multi-Omics-Profiling konnten wir die klonale Evolution bei AML mit komplexem Karyotyp (CK-AML) mit großer Präzision erforschen. Damit konnten wir neue Therapieresistenzmechanismen von LSCs aufdecken und den Mechanismus von Rezidiven verstehen (Leppä et al., Nature Genetics 2024).
Entwicklung des MAC-Scoring als zuverlässiger prädiktiver klinischer Biomarker für das Ansprechen von Patienten auf Venetoclax (BCL-2-Inhibitor): ein schneller (6 Stunden), kostengünstiger und klinisch anwendbarer Assay, der das individuelle Ansprechen von AML-Patienten auf die VEN/HMA-Therapie durchflusszytometrisch anhand der Expression von drei Mitgliedern der BCL-2-Familie in LSCs präzise vorhersagt (Waclawiczek et al., Cancer Discovery 2023). MAC-Scoring ist in verschiedenen hämatologisch-onkologischen Kliniken in Deutschland, USA und Mexiko etabliert und dient als direkte Entscheidungshilfe bei der Behandlung von AML Patienten.
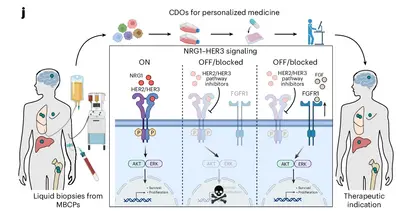
Die Behandlung und Prognose von Brustkrebs (BC) haben sich in den letzten Jahren erheblich verbessert. Dennoch ist metastasierender Brustkrebs (MBC) nach wie vor unheilbar. BC-Zellen breiten sich hauptsächlich auf Lunge, Leber, Knochen, Lymphknoten und Gehirn aus. Die Quelle der Metastasen sind zirkulierende Tumorzellen (CTCs) mit Stammzell-Eigenschaften, die Metastasen auslösen. CTCs, disseminieren vom Primärtumor und gelangen in die Blutzirkulation und von dort in alle Organe. CTCs mit Stammzell-Eigenschaften, sogenannte Metastasen-Stammzellen treiben die Metastasierung voran, die die häufigste Todesursache bei Menschen mit Krebs, einschließlich BC, ist.
→ Bedeutende Entdeckung des Trumpp-Teams: Erstmalige Isolierung von Metastasen-Stammzellen direkt aus dem Blut von Patienten und Entwicklung einer Technologieplattform zur Vermehrung von CTCs als dreidimensionale Organoide. Dies ermöglicht ihre Charakterisierung auf molekularer und funktionaler Ebene und die Ergebnisse unterstützen klinische Präzisions-Onkologieprogramme am NCT Heidelberg.
Erster experimenteller Nachweis, dass CTCs aus dem Blut von Brustkrebs-Patientinnen Metastasen initiieren, und Identifizierung von CD44+MET+CD47+ CTCs als Treiber von Knochen- und Lungenmetastasen bei Brustkrebs (Baccelli et al., Nature Biotechnology 2013).
Entwicklung einer CTC-basierten 3D-Organoid-Plattform zur Vermehrung von CTCs aus peripherem Blut von Patientinnen: Aufklärung der Schlüsselbedeutung des NRG1-HER2/3 Signalwegs für CTCs. Entdeckung einer zellulären Plastizität, die den FGFR1 Rezeptor überexprimiert um einer Abtötung durch HER2/3 Therapie zu entgehen (Würth et al., Nature Cancer 2025; Schwerd-Kleine et al., Int J of Cancer 2025).
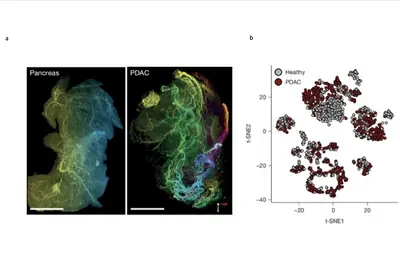
Das duktale Pankreaskarzinom (PDAC) entsteht in den Zellen, die die Pankreasgänge auskleiden. Es wird oft erst spät diagnostiziert und ist schwer zu behandeln, wobei die Gesamt-5-Jahres-Überlebensrate bei nur etwa 10 % liegt. PDAC ist durch ein desmoplastischen Stroma mit hypertrophen Nerven charakterisiert. Es ist dringend notwendig neue Behandlungsschemata zu entwickeln, um diese schwerwiegende Krebserkrankung effizienter zu bekämpfen.
→ Bedeutende Entdeckung des Trumpp-Teams: Identifizierung von Therapieresistenz-Signalwegen und Aufdeckung der Wechselwirkung zwischen peripheren Nerven und Bauchspeicheldrüsenkrebs als neuartiges therapeutisches Ziel, wodurch neue Behandlungskonzepte für PDAC erschlossen wurden.
Identifizierung des CYP3A5 Enzyms als Resistenztreiber, der mit neuartigen Inhibitoren bekämpft werden soll (Noll et al., Nature Medicine 2016; Kuhlmann et al. Pancreas 2017).
Definition eines entzündlichen PDAC-Subtyps, der durch die unterschiedliche DNA-Methylierung des Pankreaskrebs-Genoms reguliert wird. Eine Hypomethylierung führt zur genomischen Aktivierung von bestimmten, ansonsten inaktiven Retroelementen, die eine starke Interferon Aktivierung auslösen und den hochaggressiven Tumor treiben (Espinet et al., Cancer Discovery 2021).
Das periphere Nervensystem (PNS) koordiniert die Organfunktionen bei Gesundheit und Krankheit. Die meisten Krebsarten, darunter auch PDAC, sind von PNS-Neuronen infiltriert. Die neuronalen Zellkörper befinden sich jedoch in verschiedenen PNS-Ganglien, weit entfernt von der Tumormasse. Daher fehlen in den aktuellen Gewebesequenzierungsdatensätzen Neuronen, die Krebsgewebe oder gesunde Organe innervieren. Um dieses Defizit zu beheben, entwickelte das Trump-Team die Trace-n-Seq-Methode, mit der erstmals Einzelzell-Transkriptomikdaten von innervierenden Neuronen der gesunden Bauchspeicheldrüse und von PDAC gewonnen werden konnten. Dabei zeigte sich eine auffällige Umprogrammierung der innervierenden Neuronen und Nerven durch den PDAC-Tumor, um sein eigenes Wachstum und seine Metastasierung zu fördern (Thiel, Renders et al., Nature 2025).
Das Trumpp Team konnte zeigen, dass eine neuronale Blockade (Denervierung) synergistisch mit der Taxan-vermittelten Chemo- und einer Immun-Checkpoint Blockade wirkt. Diese Erkenntnisse fließen in die neue multizentrische klinische Phase I/II Studie „Synergy“ ein, die Ende 2026 starten soll (Thiel, Renders et al., Nature 2025).
Die Arbeiten des Trumpp-Teams folgen einem stringenten translationalen Ansatz, der patientenbasierte Daten mit präklinischen Modellen verknüpft. Longitudinale Primärproben werden molekular analysiert und mit klinischen Daten integriert, um Therapieansprechen, Resistenz, Rezidivbildung und Metastasierung mechanistisch zu verstehen und in die klinische Entwicklung zurückzuführen (Reverse Translation).
→ Signature Discovery: Brückenschlag zwischen Labor und Klinik durch innovative Studien bei AML, Brust- und Bauchspeicheldrüsenkrebs
Bauchspeicheldrüsenkrebs: Leitung der Phase-I-Studie „Intensify“ zur Untersuchung von CYP3A-Inhibitoren in Kombination mit Paclitaxel/Gemcitabin (zusammen mit Prof. Springfeld, NCT Heidelberg).
Bauchspeicheldrüsenkrebs: Vorbereitung der Phase-I/II-Studie „Synergy“ zur Kombination von neuronaler Blockade mit Chemo- und Immuntherapie (zusammen mit klinischen Kollegen am Universitätsklinikum Heidelberg und anderen deutschen Krebszentren).
Brustkrebs: Zentrale Forschungsaktivität in den Brustkrebs-Registerstudien CATCH & COGNITION (mit Prof. Schneeweiss, NCT Heidelberg).
AML: Untersuchung der Wirksamkeit von PARP1-Inhibitoren und NK-Zell-Infusionen in der Phase-I/II-Studie NAKIP-AML (mit Prof. Müller-Tidow, Universitätsklinikum Heidelberg).
AML: Prospektive AML-Studien zur weiteren Validierung des MAC-Scoring und zur Entwicklung eines Diagnose-Kits mit Pharma sowie Gründung eines Start-up-Unternehmens.
Ausblick:
Krebs ist kein statischer Zustand, sondern ein hochdynamischer, anpassungsfähiger Prozess, der eng mit seiner mikro- und makroskopischen Umgebung verwoben ist. Durch die gezielte Verknüpfung von Stammzellbiologie, Einzelzelltechnologien, Metastasenforschung und dem neu entstehenden Forschungsfeld der Cancer Neuroscience untersuchen wir die Mechanismen, die Tumorresistenz, Rezidivbildung und Metastasierung antreiben.
Unsere langfristige Vision ist die Entwicklung innovativer, patientenspezifischer Therapiestrategien, die gezielt jene „Stammzellprogramme“ adressieren, welche Tumorentstehung und -progression begünstigen. Von der prädiktiven Therapieansprache bei AML über die bahnbrechende neuronale Intervention beim Pankreaskarzinom bis hin zur funktionellen Charakterisierung zirkulierender Tumorzellen beim Mammakarzinom eröffnet unsere Forschung neue therapeutische Perspektiven über Tumorentitäten hinweg.
Mit jeder Erkenntnis kommen wir dem Ziel näher, bislang unheilbare Krebserkrankungen in langfristig kontrollierbare – und letztlich heilbare – Krankheiten zu überführen.
HI-STEM gGmbH:
Neben seiner Funktion als Leiter der Abteilung für Stammzellen und Krebs ist Prof. Trumpp auch Geschäftsführer der Heidelberg Stem Cell Technology and Experimental Medicine (HI-STEM gGmbH), die im Hauptgebäude des DKFZ untergebracht ist. Klicken Sie hier für weitere Details.
Wissenschaftliche Leitung:
Prof. Dr. Andreas Trumpp hat über 200 Artikel in Fachzeitschriften mit Peer-Review veröffentlicht, die mehr als 40.000 Mal zitiert wurden, und hat einen H-Index von 94. In den Jahren 2019 und 2022 wurde er von Web of Science als hochzitierter Forscher (Top 1 % weltweit) ausgezeichnet. Er erhielt 2020 den Deutschen Krebspreis und 2022 einen ERC Advanced Grant und ist Mitglied mehrerer wissenschaftlicher Beiräte und Ausschüsse wissenschaftlicher Gesellschaften. Mehr als 16 seiner Teammitglieder leiten heute als Gruppenleiter oder Professoren ihre eigenen Forschungsgruppen, und viele seiner Teammitglieder haben führende Positionen in der Industrie inne. Den Lebenslauf von Prof. Trumpp finden Sie hier.
Team
-

Prof. Dr. Andreas Trumpp
Abteilungsleiter "Stammzellen und Krebs", Geschäftsführer des Stammzellinstituts "HI-STEM gGmbH"
-

Dr. Hamed Alborzi Nia
HI-STEM Nachwuchsgruppe "Mechanisms of Cell Death and Drug Resistance"
-

Dr. Nesrine Aroua
Wissenschaftlerin
-
Lucas Barea Moya
-
Tamara Benz
Wissenschaftlerin
-
Moritz Berg
-

Ines Bergerweiss
Doktorandin
-

Katharina Block
Auszubildende Technische Assistentin
-
Julia Bulkescher
Technische Assistentin
-
Samuele Cesaro
-

Tasneem Cheytan
Doktorandin
-

Dr. Sascha Henry Conic
Wissenschaftler
-
Jule Dettweiler
Student Assistant
-

Dr. Elisa Donato
Wissenschaftlerin
-
Daria Doncevic
-
Anna Edenhofer
Doktorandin
-
Dr. Mostafa Ejtehadifar
Wissenschaftler
-
Andrea Garcia Yuste
-

Dr. Lissy Gross
Wissenschaftlerin
-
Florian Grünschläger
-

Isabell Guckes
Master Student
-

Dr. Ewgenija Gutjahr
Wissenschaftlerin
-
Pablo Henneman
Doktorand
-

Dr. Kim Hoa Ho
Wissenschaftlerin
-

Dr. Frank Yi-Tao Huang
MD und Doktorand
-
Marlene Hühn
Doktorandin
-
Lea Jopp-Saile
-
Nina Sophie Kruse
-
Erika Krückel
Leitung Administration HI-STEM
-

Andrea Kuck
Technische Assistentin
-
Jana Kunder
-

Dr. Christina Köhler
Klinische Wissenschaftlerin
-

Yara Lackousha
Doktorandin
-

Sarah Lang
Doktorandin
-
Aino-Maija Leppä
-
Estefania Isabella Leth
-

Jennifer Lewis
Doktorandin
-

Dr. Shuiping Lin
Wissenschaftlerin
-

Sabrina Lohr
Technische Assistentin
-

Dr. Maria Puschhof
HI-STEM Nachwuchsgruppe "Bioinformatik"
-

Simon Renders
Klinischer Wissenschaftler
-
Emma Röhm
Wissenschaftliche Hilfskraft
-
Darius Schenk
Master Student
-

Sebastiaan Schieven
Wissenschaftler
-
Dr. David Schlütermann
-

Dominique Schulz
Doktorandin
-
Fabian Sieker
Master Student
-

Markus Sohn
Technischer Assistent
-

Dr. Shubhankar Sood
HI-STEM Nachwuchsgruppe "Global Precision Medicine (GPM) Translational Research Group"
-

Dr. Martin Sprick
HI-STEM Forschungsgruppe "Stammzellen und Metastasen"
-

Dr. Patrick Stelmach
Klinischer Wissenschaftler
-

Natalie Stumpf
Technische Assistentin
-

Karolin Stumpf
Doktorandin
-

Vera Thiel
Wissenschaftlerin
-
Vera Thiel
-

Dr. Marc Thier
HI-STEM Nachwuchsgruppe "Chronically progressive neurodegenerative diseases"
-
Dr. Aset Ceren Thier
-

Beatrice Tröster
Doktorandin
-
William Wachter III
-

Alexander Waclawiczek
Wissenschaftler
-

Bettina Walter
Technische Assistentin
-

Rebecca Weber
Technische Assistentin
-

Dr. Jennifer Wischhusen
Wissenschaftlerin
-
Dagmar Wolf
Persönliche Assistentin
-

Nils Wörner
Doktorand
-

Dr. Roberto Würth
Wissenschaftler und Team Leader
-
Umut Yildiz
-

Petra Zeisberger
Technische Assistentin
-

Dr. Basak Özata
Business Development
Ausgewählte Publikationen
Thiel, V., Renders, S., et al.,
Würth, R., et al.,
Leppä, AM., et al.,
Waclawiczek, A., et al.,
Hernandez-Malmierca, P., et al.,
Espinet, E., et al.
Raffel, S. et al.
Cabezas-Wallscheid, N., et al.,
Essers, M., et al.,
Wilson, A., et al.,
Offene Positionen
Unsere Arbeitsgruppe ist stets auf der Suche nach motivierten Wissenschaftler:innen.
Informationen zu Karriereprogrammen am DKFZ finden Sie unter Cancer Research Academy at DKFZ. Bei direkten Anfragen senden Sie bitte Ihre Bewerbung per E-Mail an office-trumpp@dkfz-heidelberg.de. Fügen Sie Ihrer Bewerbung ein Anschreiben mit Angabe Ihrer Forschungsinteressen, Ihren Lebenslauf mit einer vollständigen Liste Ihrer Veröffentlichungen sowie die Kontaktdaten von drei Referenzpersonen bei.
Funding
Unsere Forschung wird großzügig unterstützt von:

Kontaktieren Sie uns

Prof. Dr. Andreas Trumpp
Abteilungsleiter "Stammzellen und Krebs", Geschäftsführer des Stammzellinstituts "HI-STEM gGmbH"
